TRAVAUX
DIRIGES : « ATOMES ET MOLECULES » - Cours de Thierry Briere
Tous les cours, sujets
d’examens et les corrigés des TD seront
accessibles sur le site : www.chimie-briere.com
Série 6 :
Electronégativité de Pauling
- Liaisons Polarisées - Moments dipolaires
|
|
E liaison (kJ.mol-1) |
longueur liaison (A°) |
Moment dipolaire (D) |
|
H2 |
435 |
|
|
|
F2 |
155 |
|
|
|
Cl2 |
242 |
|
|
|
Br2 |
|
|
|
|
HF |
566 |
0,92 |
1,82 |
|
HCl |
431 |
1,27 |
1,08 |
|
HBr |
|
1,42 |
0,79 |
|
HI |
|
1,61 |
0,38 |
Exercice 1
:
1) Déterminer les électronégativités
selon Pauling des atomes Fet Cl. On prendra k
= 2,2 pour H.
On sait que HF et HCl sont des acides se dissociant en X-
et H+, F et Cl sont donc plus électronégatif que H.
On peut calculer l'électronégativité de
Pauling en utilisant soit la moyenne arithmétique, soit la moyenne géométrique.
Moyenne arithmétique : DX2
= { EAB - 1/2 ( EAA+EBB ) } / k
Si on utilise les énergies en
kJ.mol-1 : k = N e / 1000 = F / 1000 = 96,5
(XF
– XH)2 = { EHF - 1/2 ( EHH+EFF)}
/ k
(XF
– XH)2 = { 566 - 1/2 (
435+155)} / 96.5 = 2,808
(XF
– XH) = 1,676
XF = 2,2 + 1,676 = 3,88
(XCl
– XH)2 = { EHCl - 1/2 ( EHH+EClCl)}
/ k
(XCl
– XH)2 = { 431 - 1/2 (
435+242)} / 96.5 = 0,958
(XCl
– XH) = 0,979
XCl = 2,2 + 0,979 = 3,18
Moyenne géométrique : DX2
= { EAB - ( EAA*EBB )1/2 } / k
Si on utilise les énergies en
kJ.mol-1 : k = N e / 1000 = F / 1000 = 96,5
(XF
– XH)2 = { EHF - ( EHH+EFF) } 1/2/
k
(XF
– XH)2 = { 566 - (
435*155) 1/2 }/ 96.5 = 3,17
(XF
– XH) = 1,78
XF = 2,2 + 1,78 = 3,98
(XCl
– XH)2 = { EHCl - ( EHH*EClCl)1/2
} / k
(XCl
– XH)2 = { 431 - (
435*242)1/2 } / 96.5 = 1,104
(XCl
– XH) = 1,05
XCl = 2,2 + 1,05 = 3,25
Exercice 2 :
Calculer les pourcentages ioniques des
liaisons suivantes :
H ---- Cl m = 1,08 D d
= 1,27 A°
H ---- Br m = 0,79 D d
= 1,42 A°
H ---- I m = 0,38 D d
= 1,61 A° (1 D = 0,333 10-29
C . m)
Comparez avec les valeurs obtenues par les formules
de Pauling et de Haney-Smith
Pauling : %IAB
= 100 ( 1 - exp(- (DX)2/4))
Haney-Smith :
%IAB = 16 IDXI + 3,5 IDXI2
m = d * d
d = m / d
d en Coulomb si m
en C.m et d en m
%I = d / e * 100
|
|
m (D) |
d(A°) |
d = m / d (C) |
%I |
|
H ---- F |
1,82 |
0,92 |
6,59E-20 |
41 |
|
H ---- Cl |
1,08 |
1,27 |
2,83E-20 |
18 |
|
H ---- Br |
0,79 |
1,42 |
1,85E-20 |
12 |
|
H
---- I |
0,38 |
1,61 |
7,86E-21 |
5 |
On trouve dans les tables les électronégativités de Pauling de F, Cl, Br et I
XF
= 3,98 è DX
= XF – XH = 3,98 – 2,2 = 1,78
XCl
= 3,16 è DX
= XCl – XH = 3,16 – 2,2 = 0,96
XBr
= 2,96 è DX
= XBr – XH = 2,96 – 2,2 = 0,76
XI = 2,66 è DX = XI – XH = 2,66 – 2,2 = 0,46
|
|
X |
DX |
%I
Pauling |
%I
Haney-Smith |
%I m
et d |
|
F |
3,98 |
1,78 |
55 |
40 |
41 |
|
Cl |
3,16 |
0,96 |
21 |
19 |
18 |
|
Br |
2,96 |
0,76 |
13 |
14 |
12 |
|
I |
2,66 |
0,46 |
5 |
8 |
5 |
La
formule empirique de Haney-Smith est très satisfaisante.
Exercice 3 :
La
molécule SO2 a une géométrie en V ; l’angle des deux liaisons
S-O est de 119°. Son moment dipolaire mesuré est de 1,65 D (1 D = 0,333 10-29
C . m). Donner la structure de Lewis de cette molécule. Montrer qu’on peut la
décrire par deux structures mésomères obtenues soit en “ excitant ”
S, soit en “ excitant ” O. La longueur de liaison expérimentale est
de 1,43 A°. Comparer à la valeur calculée. Conclusion ? Calculer le pourcentage
d’ionicité de ces liaisons. Calculer les charges partielles portées par chaque
atome.
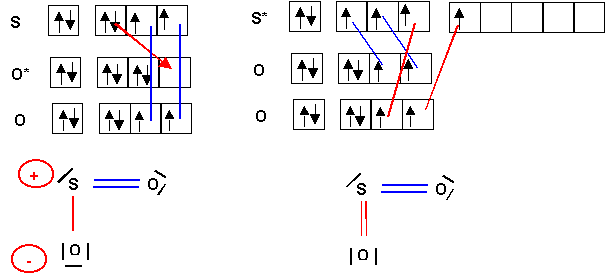
La géométrie de la molécule est bien du type AX2E en forme de V avec un angle proche de 120°.
La valeur expérimentale de l'angle 119° est justifiée par la présence du doublet libre qui est pratiquement compensée par celles des deux doubles liaisons, l'effet du doublet libre l'emporte tout de même et l'angle est très légèrement inférieur à 120°.
Si
on examine les deux formes mésomères on accordera un poids statistique plus
important à la forme à deux doubles liaisons et non chargée puisqu'elle possède
à la fois d'avantage de liaisons et moins de charges que l'autre forme.
Remarque : la règle de l'octet n'est pas respectée pour cette forme alors qu'elle l'est pour l'autre, mais cette règle ne s'applique strictement qu'aux éléments de la deuxième période ce qui n'est pas le cas du soufre.
On
peut aussi s'intéresser à la longueur expérimentale des liaisons.
Z*S = 5,45 , n*S = 3 , Z*O = 4,55, n*O = 2 , RS = 1,024 A° ; RO = 0,71 A° soit pour les longueurs des liaisons S - O :
Simple 1,72 A° - Double : 1,48 A° - Triple 1,34 A°
La
longueur réelle de la liaison de 1,43 A° est légèrement plus courte que la
valeur approchée calculée pour la liaison double SO. Cela est en accord avec
l'hypothèse que la forme mésomère à doubles liaisons est bien la forme la plus
représentative de la molécule réelle. Nous verrons que le raccourcissement
observé peut être attribué à la forte polarité de la liaison SO.
Calcul
des charges partielles et du pourcentage d'ionicité :
Les
moments dipolaires des liaisons s'ajoutent vectoriellement, leur résultante est
le moment dipolaire global de la molécule. Ici le moment dipolaire global est
connu et nous cherchons le moment dipolaire partiel d'une liaison SO qui nous
permettra ensuite de déterminer le pourcentage d'ionicité de la liaison.
Nous
négligerons le moment dipolaire partiel du au doublet libre qu'il est
impossible d'évaluer.
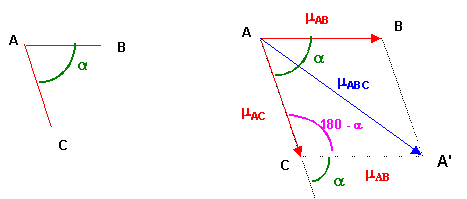
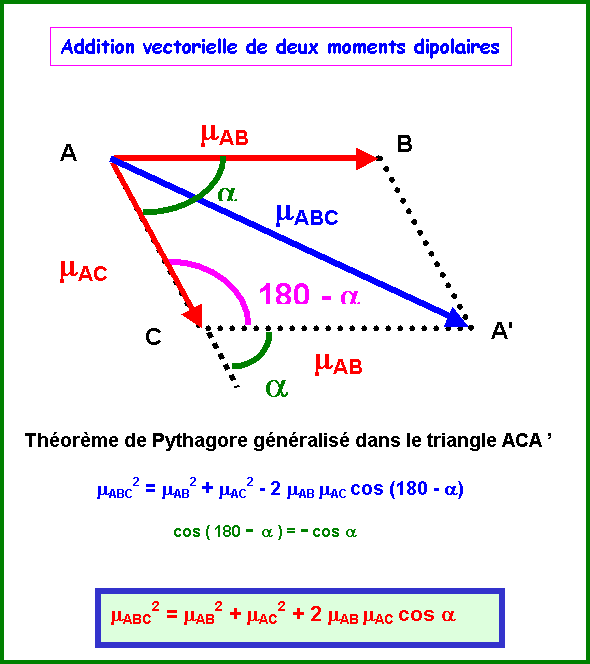
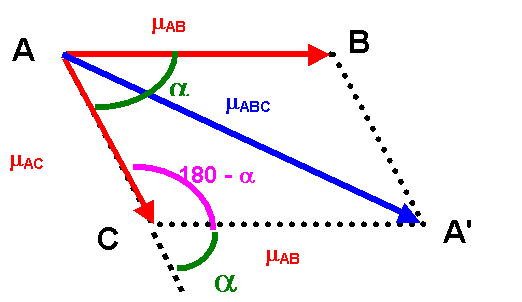
Théorème
de Pythagore généralisé :
Triangle ACA'
mABC2 = mAB2 + mAC2 - 2 mAB mAC cos (180 - a)
mABC2 = mAB2 + mAC2 + 2 mAB mAC cos a
Ici on à de plus mAB = mAC = mSO
mSO22 = mSO2 + mSO2 + 2 mSO mSO cos a
mSO22 = 2 mSO2 + 2 mSO2 cos a
mSO22 = 2 mSO2 ( 1 +
cos a )
Soit mSO2 = mSO22 / 2 ( 1 +
cos a )
Application
numérique :
mSO2 = 1,652 / 2 ( 1 + cos 119 ) = 2,64
mSO = 1,625 D
%ISO = 20,8 *
1,625 / 1,43 = 23,6 %
Soit d = 0,24 e = 3,68 10-20 C
Cette
liaison 24 % ionique est plus polarisée que la liaison H-Cl pour laquelle le
pourcentage d'ionicité n'est que de 17 %, cette forte ionicité justifie le
raccourcissement de la liaison observé.
On
peut le vérifier grâce à la formule empirique : LAB = RA
+ RB – 9 DX (R en pm)
Ici
XO = 3,44 et XS = 2,58 (voir tables) soit DX = 0,86
RS = 1,024 A° =102,4 pm ; RO = 0,71 A°= 71 pm
Soit
LSO = 102,4 + 71 – 9 * 0,86 = 165,7 pm = 1,657 A°
La
liaison est double donc LSO = 0.86 * 1,657 = 1,425 A°
On
retrouve bien la valeur expérimentale de 1,43 A°.
Exercice 4 :
Sachant que le moment dipolaire partiel de liaison mN-O est de 0.15 D :
a) calculer le moment dipolaire global de l’ion NO3-.
b) calculer le moment dipolaire global de la molécule NO2 (a = 134° voir précédemment).
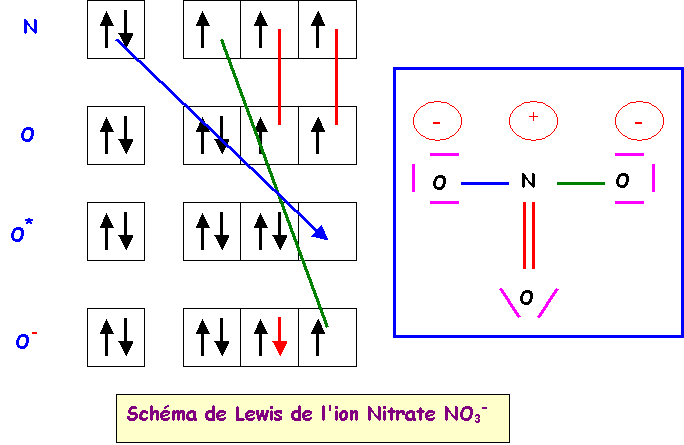
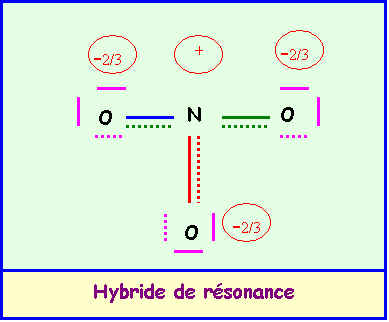
La géométrie de cet ion est du type AX3
parfaitement symétrique, triangle équilatéral parfait avec trois angles de 120°
exactement. En raison de cette symétrie parfaite le moment dipolaire global de
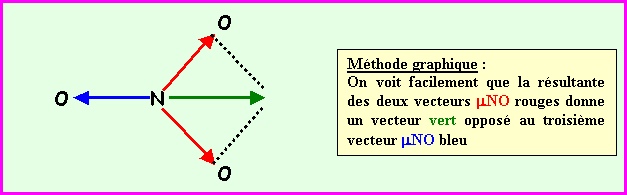
NO3- sera nul, en effet la résultante de deux des
vecteurs mNO donne un
vecteur exactement opposé au troisième vecteur mNO
et il y a donc annulation du moment dipolaire global. Cela se voit facilement
graphiquement mais on peut aussi le vérifier par le calcul.
Dans notre cas : a = 120° et cos a = -0,5, de
plus, mAB = mAC
mABC2 = mAB2 + mAC2 + 2 mAB mAC cos a
mABC2 = 2 mAB2 + 2 mAB2 * -0,5
mABC2 = 2 mAB2 - mAB2 = mAB2
mABC = mAB
On
obtient bien un vecteur opposé au troisième è Résultante totale
nulle.
b) calculer le moment dipolaire global de
la molécule NO2 (a = 134°).
Dans ce cas : a = 134° et cos a = -0,695, de
plus, mAB = mAC
mABC2 = mAB2 + mAC2 + 2 mAB mAC cos a
mABC2 = 2 mAB2 + 2 mAB2 cos a = 2 mAB2 ( 1 - cos a )
mABC2 = 2 * 0,15 * ( 1 + 0,695 ) = 0,5085
mABC = 0,713 D
mNO2 = 0,713 D
Exercice 5
:
Une seule des trois molécules CO2 , CS2 et COS possède un moment dipolaire permanent.
Laquelle ? Pourquoi ? Quel est le sens de ce moment dipolaire ?
CO2 CS2 et COS sont iso électroniques et possèdent donc une géométrie identique de type AX2, les trois molécules sont linéaires. Par annulation mutuelle des moments de liaison CO2 et CS2 possèdent un moment dipolaire global nul. Seul COS possédera donc un moment dipolaire permanent. O étant plus électronégatif que S il sera dirigé vers l’atome d’Oxygène.
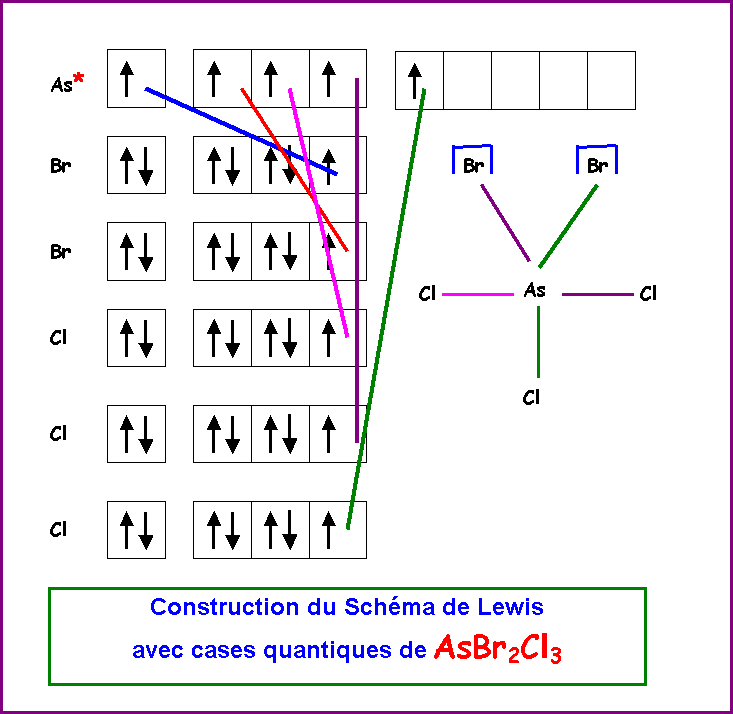
Exercice 6
Soit
le composé de formule AsBr2Cl3
- Donner son schéma de Lewis
- Montrer qu'il existe trois isomères différents de ce composé.
- Donner une représentation spatiale de chacun des trois isomères.
- Classer ces trois isomères par ordre de stabilité croissante.
- Evaluer le moment dipolaire de chacun des trois isomères.
Electronégativités
dans l'échelle de Pauling :
As ( X = 2,2 ) - Br : ( X = 2,96 ) - Cl ( X = 3,16 )
Moments dipolaires des liaisons
As - Cl : m = 1,3 D -
As - Br : m = 1,6 D (
1 D = 0,333 10-29 C.m )
1)
Montrer qu'il existe trois isomères différents de ce
composé.
La géométrie autour de As est du type
AX5 soit une bi-pyramide à base triangle, les sommets ne sont pas
équivalents, il existe trois sommets équatoriaux et deux sommets axiaux.
On
pourra donc placer les atomes latéraux de trois manières différentes :
Isomère A : 2 Bromes axiaux et 3 chlores équatoriaux.
Isomère B : 1
Brome axial, 1 Brome équatorial, 1 chlore équatorial et 2 chlores axiaux
.
Isomère C : 2
Bromes équatoriaux , 2 Chlores axiaux et 1 Chlore équatorial.
2)
Donner une représentation spatiale de chacun des trois isomères.
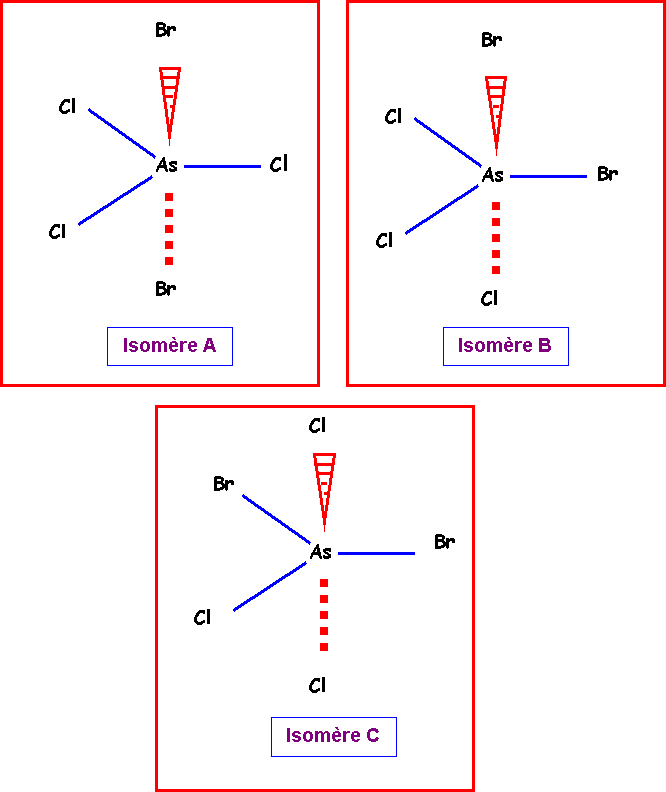
3)
Classer ces trois isomères par ordre de stabilité
croissante.
Electronégativités
dans l'échelle de Pauling :
As ( X = 2,2 ) - Br : ( X = 2,96 )
- Cl ( X = 3,16 )
Liaison As
- Br
:
Br plus
électronégatif que As attire les électrons de la liaison vers
lui, la liaison AsBr est donc
polarisée.
Liaison As
– Cl :
Cl plus
électronégatif que As attire les électrons de la liaison
vers lui, la liaison AsCl est donc
polarisée.
Le
Chlore étant plus électronégatif que le Brome la polarisation des liaisons AsCl est plus importante que celle des
liaisons AsBr.
Conséquences :
-
les
doublets des liaisons AsCl sont plus
éloignés de As que ceux des
liaisons AsBr.
-
Les
charges partielles portées par les atomes sont plus importantes dans les
liaisons AsCl que dans les
liaisons AsBr
-
Le
moment dipolaire de la liaison AsCl (1,6 D) est
plus important que celui de la liaison AsBr (1,3 D).
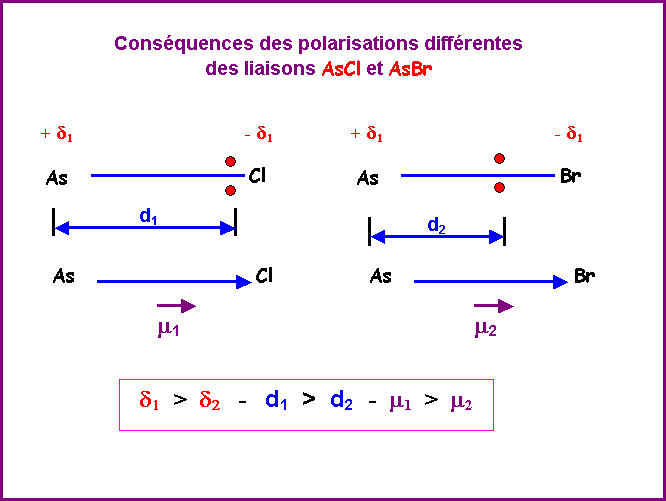
L'existence de ces dissymétries va se répercuter
sur les stabilités relatives des trois isomères. L'isomère le plus stable sera
celui pour lequel les répulsions entre doublets seront minimales, c'est à dire
celui pour qui les doublets seront le plus éloignés de l'atome central. L'atome
le moins électronégatif (ici Br) se placera donc préférentiellement en
positions équatoriales (angles de 120°) plutôt qu'en positions axiales (angles
de 90° uniquement).
L'ordre de stabilité croissante est
donc :
Isomère A < isomère B < isomère C
( 2 Br axiaux) <
(1 Br
équatorial) < (2 Br équatoriaux )
Remarque :
Les
atomes peu électronégatifs attirant peu les électrons sont de gros atomes
Les
atomes très électronégatifs attirant fortement les électrons sont de petits
atomes.
Le raisonnement plus simple (mais moins rigoureux)
consistant à se baser sur la taille de l'atome en disant que les gros atomes se
placent préférentiellement en position équatoriale car ils y trouvent plus de
place (encombrement stérique) conduit donc au même résultat qualitatif.
4)
Evaluer le moment dipolaire de chacun des trois isomères.
Isomère A :
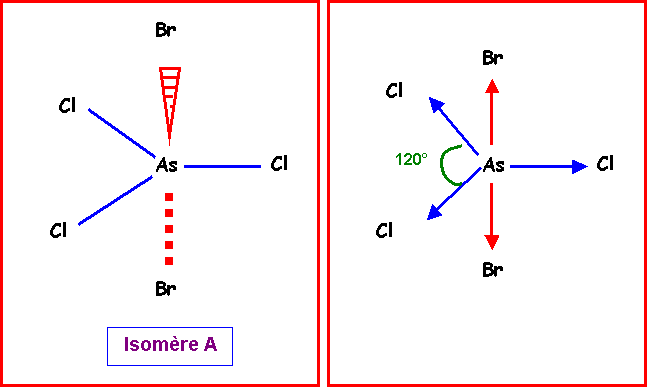
On voit facilement sur la
représentation spatiale que les deux vecteurs correspondant aux moments
dipolaires des liaisons AsBr s'annulent mutuellement.
De plus, la résultante de deux vecteurs
mAsCl donne un vecteur opposé au troisième.
Les trois vecteurs mAsCl s'annulent donc les uns les autres et leur
résultante est nulle.
On peut le vérifier par le calcul :
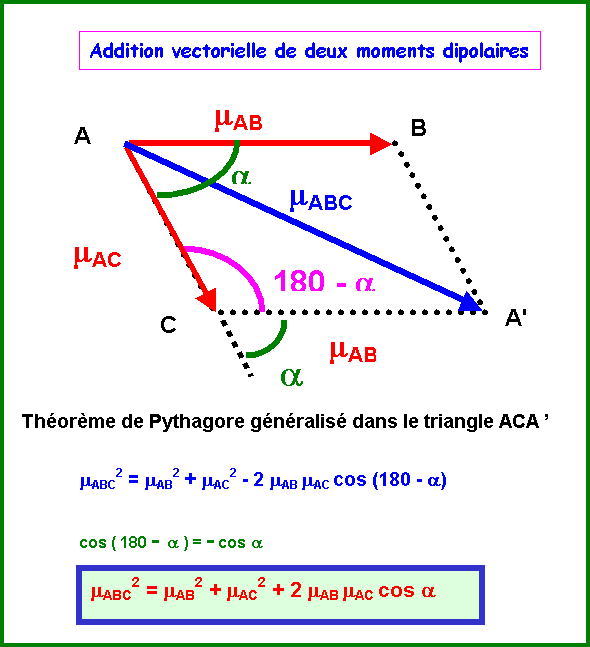
Dans le cas qui nous intéresse :
mAB
= mAC = mAsCl et a = 120°
mABC2 = mAB2 + mAC2 + 2 mAB mAC cos a
mABC2 = mAsCl2 + mAsCl2 + 2 mAsCl mAsCl cos 120
mABC2 = 2 mAsCl2 ( 1 + cos 120 )
mABC2 = 2 mAsCl2 ( 1 - 0,5 )
mABC2 = mAsCl2
mABC = mAsCl
La somme des deux vecteurs mAsCl équatoriaux
donne bien un vecteur opposé au troisième.
Finalement le moment dipolaire global
de l'isomère A est donc nul.
Isomère B :
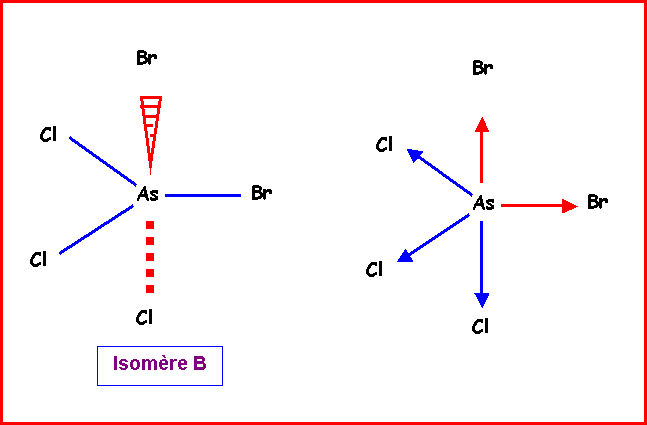
Nous venons de voir qu'on pouvait
remplacer les deux vecteurs mAsCl équatoriaux
par un seul de sens opposé au vecteur mAsBr équatorial. On peut ensuite
additionner les deux vecteurs mAsBr orthogonaux entre eux et les deux
vecteurs mAsBr orthogonaux entre eux également.
Soit :
mAB
= mAC = mAsCl et a = 90°
mABC2 = mAB2 + mAC2 + 2 mAB mAC cos a
mABC2 = mAsCl2 + mAsCl2 + 2 mAsCl mAsCl cos 90
mABC2 = 2 mAsCl2
mABC = Ö2 mAsCl
De même pour les vecteurs mAsBr
mABC = Ö2 mAsBr
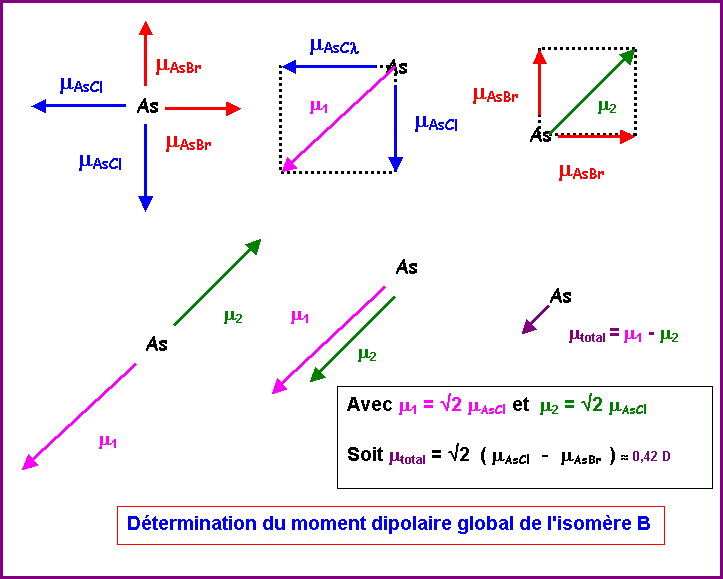
Il suffit ensuite d'additionner les
deux résultantes partielles (qui sont de sens opposé) pour obtenir le moment
dipolaire global de l'isomère B.
m = Ö2 ( mAsCl - mAsBr ) = Ö2 ( 1,6 - 1,3
) » 0,42 D
Isomère C :
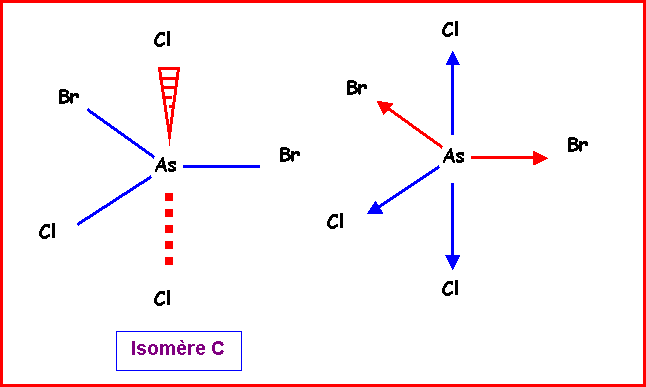
Ce cas est beaucoup plus simple que le
précédant.
Les deux vecteurs mAsCl axiaux s'annulent mutuellement.
On remplace les deux vecteurs mAsBr
équatoriaux
par un seul de sens opposé au vecteur mAscl équatorial.
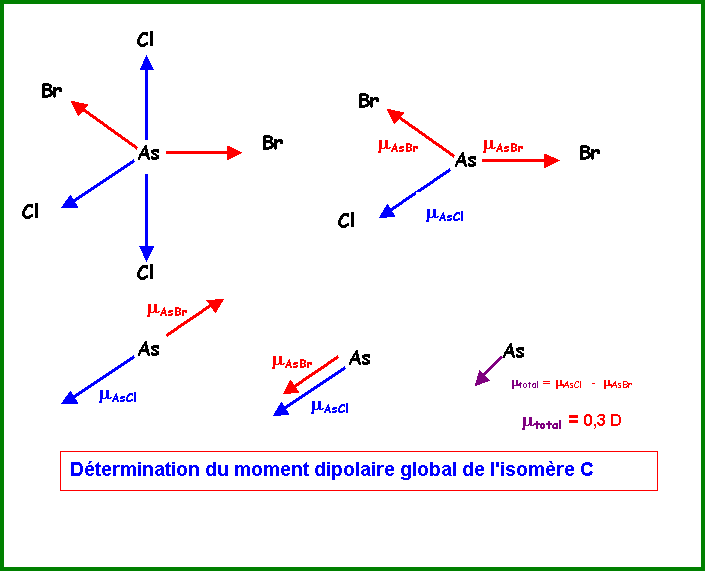
La résultante est donc mtotal = mAsCl - mAsBr
=
1,6 - 1,3 = 0,3 D
Résumé
:
|
Isomère |
Moment dipolaire global (en Debye) |
|
A |
0 |
|
B |
0,42 |
|
C |
0,3 |
Exercice 7
La molécule d'eau possède un moment dipolaire global m H2O = 1,845 D.
L’angle des liaisons O-H dans la molécule d’eau étant de 104,5 ° et la longueur de la liaison O - H de 0,95 A°.
a) calculer le caractère ionique partiel de la liaison O - H.
Ce fort moment dipolaire fait de l'eau un solvant très polaire.
mABC2 = mAB2 + mAC2 + 2 mAB mAC cos a
mH2O2 = mOH2 + mOH2 + 2 mOH mOH cos a
mH2O2 = 2 mOH2 (1+ cos a)
mOH2 = mH2O2 / 2 (1+ cos
a)
mOH2 = 1,8452
/ 2 (1+ cos 104,5 = 2,27
mOH = 1,51 D = 5,018 10-30
C.m
m = d * d
d = m / d = 5,018 10-30 / 0,95 10-10 =
5,28 10-20 C = 0,33 e
La liaison OH est ionique à 33%
b)
Il a pour autre
conséquence que les points d'ébullition et de fusion de l'eau sont anormalement
élevés. Justifier ce fait expérimental.
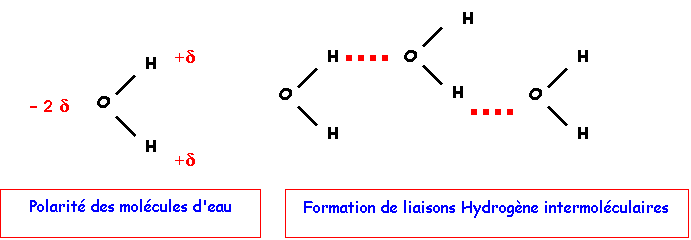 Dans l'eau, il
existe des liaisons Hydrogène inter moléculaires qui unissent les molécules
entre elles. Les point d'ébullition et de fusion sont donc fortement augmentés.
Dans l'eau, il
existe des liaisons Hydrogène inter moléculaires qui unissent les molécules
entre elles. Les point d'ébullition et de fusion sont donc fortement augmentés.
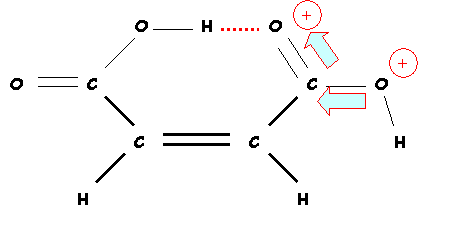
Exercice 8 : Acide maléïque et acide fumarique
Ces
deux composés isomères ont la même formule brute C4H4O4
et présentent les structures suivantes :
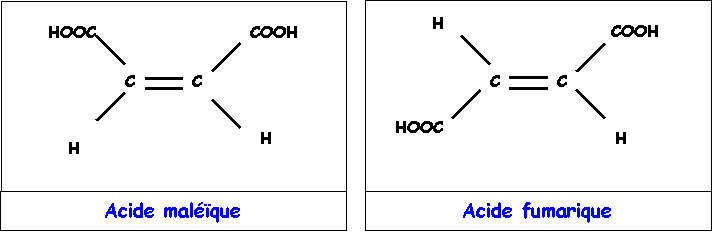
1) En supposant que le groupement COOH soit très électronégatif (et donc plus électronégatif que C) et en négligeant la polarité des liaisons C - H, montrer qualitativement que les moments dipolaires globaux des deux isomères doivent être très différents l'un de l'autre. Quel est l'isomère possédant le moment dipolaire le plus élevé? Quel est l'isomère possédant le moment dipolaire le plus faible?
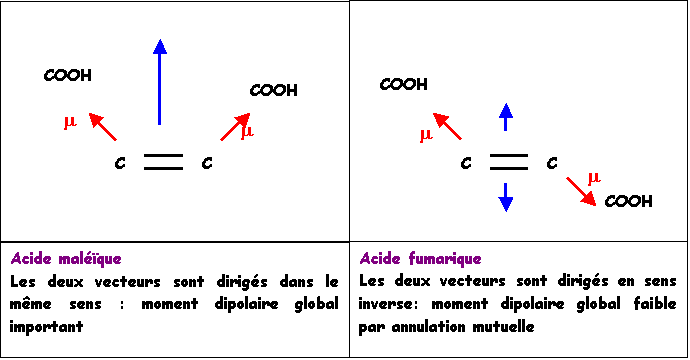
2) Solubilité dans l'eau des
acides maleïque et fumarique
Sachant que les molécules polaires sont très solubles dans les solvant polaires alors que les substances peu polaires le sont beaucoup moins, prévoir lequel des deux acides maleïque ou fumarique est le plus soluble dans l'eau.
L'acide maléique polaire sera le plus
soluble dans l'eau.
3) Point de fusion des acides maleïque et fumarique
L'un de ces deux acides possède un point de fusion de 130°C et l'autre un point de fusion de 226°C. Justifiez cette forte différence et attribuez son point de fusion à chaque isomère.
Il existe ici des liaisons Hydrogène
intramoléculaires dans l'acide maléique qui n'existent pas pour l'acide
fumarique. Ces liaisons intramoléculaires provoquent un fort abaissement des
températures de changement d'état. Les liaisons se faisant à l'intérieur de la
même molécule, les molécules sont plus individualisées. Inversement l'éxistence
de liaison inter-moléculaires (entre molécules différentes) dans l'acide
fumarique augmente ses températures de changement d'état.
Acide maléique : liaisons H
intra-moléculaires è Point de
Fusion abaissé Tf = 130°C
Acide fumarique : liaisons H
inter-moléculaires è Point de
Fusion élevé Tf = 226°C
4) Constantes d'acidité des acides maleïque et fumarique
L'un des deux isomères possède les pKa suivants : pK1 = 3 et pK2 = 4,4
L'autre isomère possède les pKa suivants : pK1 = 1,9 et pK2 = 6,2
On voit que l'un des deux composés possède simultanément le pK1 le plus petit et le pK2 le plus grand. Justifier ce fait expérimental par un/des schéma(s).
Attribuer a chaque isomère les valeurs de ces deux pKa.
L'acide
maléique à liaison Hydrogène intramoléculaire possède à la fois le pK1
le plus petit et le pK2 le plus élevé.
Acide
maléïque : pK1 = 1,9 et pK2 = 6,2
Acide
fumarique : pK1 = 3 et pK2 = 4,4
Atome d'hydrogène
lié à deux oxygènes, donc moins libre. Acidité diminuée è pKa augmente
La
liaison H fait apparaître une charge positive sur l'atome d'oxygène
concerné. Ce
déficit électronique se répercute sur l'autre atome d'Oxygène. Atome
d'hydrogène lié a un atome déficitaire en électrons donc plus facile à
libérer. Acidité
augmentée è pKa diminue