La
rotation autour de la liaison simple CC est libre.
Il existe donc
une infinités de conformations différentes.
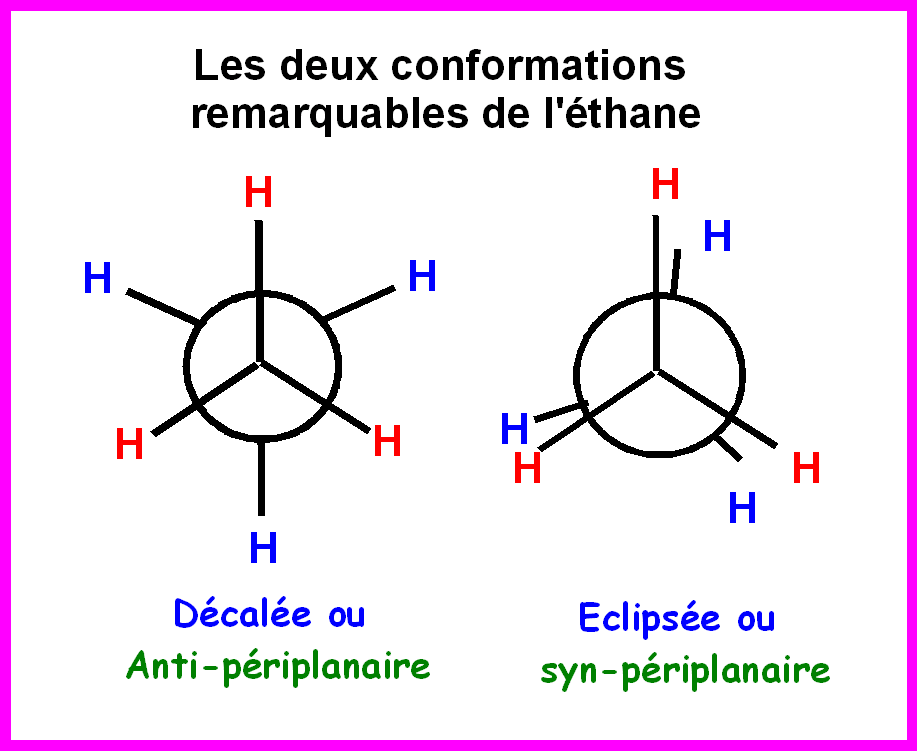
Parmi
l'infinité des conformations possibles, deux d'entre-elles
possèdent une géométrie remarquable :
|
|
|
|
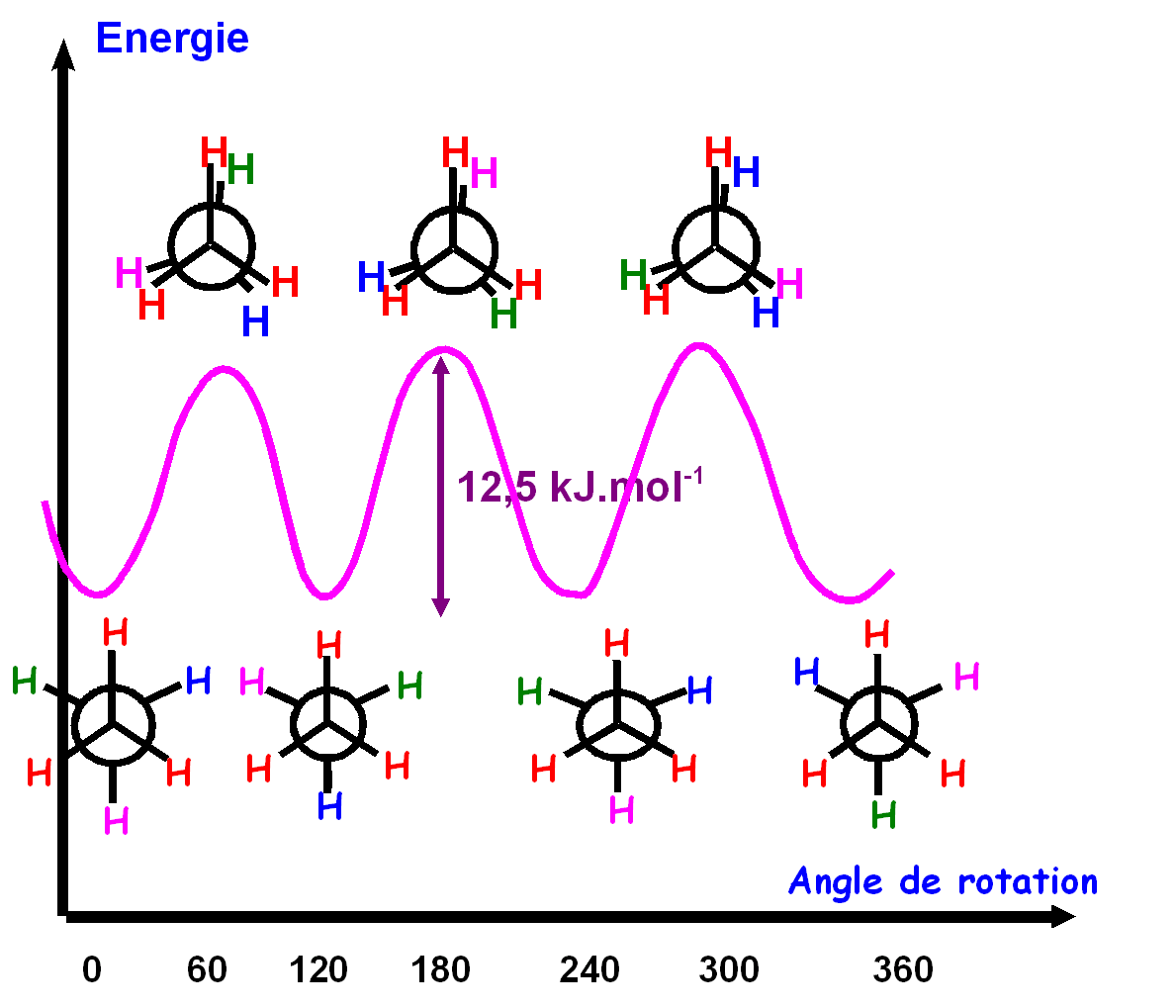
Aspect énergétique :
D’un
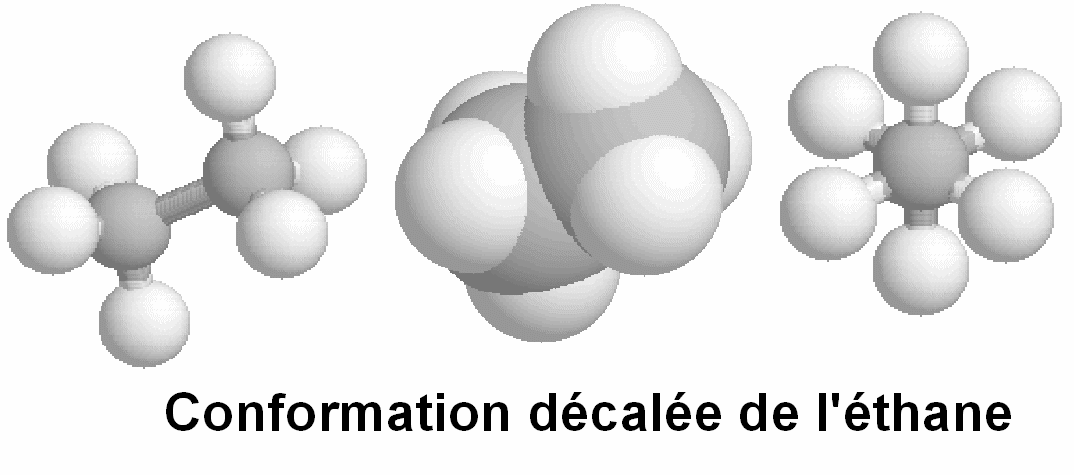
point de vue énergétique, la forme décalée
correspond à un minimum et inversement la forme éclipsée
correspond à un maximum.
Cela s’explique par les
répulsions électroniques qui sont minimales dans la
forme décalée et maximales dans la forme
éclipsée.
L’écart énergétique
entre les deux valeurs extrêmes est de l’ordre de 12
kJ.mol-1 pour l’éthane.
La courbe de
variation de l'énergie potentielle de la molécule en
fonction de l'angle dièdre entre les
liaisons C-H a l'allure suivante :