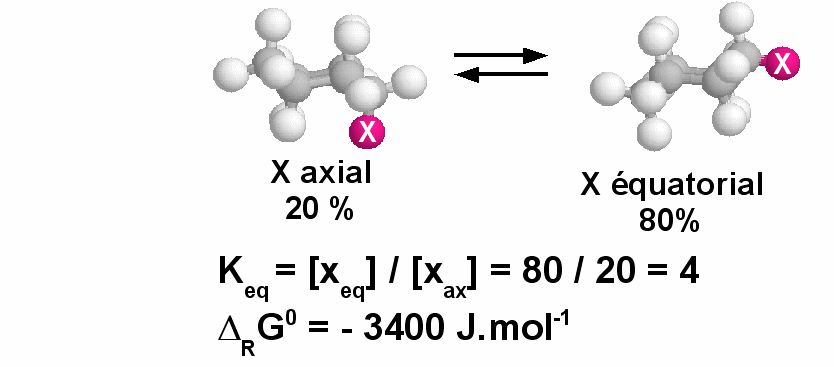
Si on substitue un des
hydrogènes du cyclohexane par exemple par un méthyle,
il va exister un équilibre entre les deux formes chaises,
l'une avec le substituant en équatorial et l'autre avec le
substituant en axial.
On observe à tempérarure
ordinaire, qu'en moyenne, 80% des molécules sont sous la
conformation X équatorial et 20% en conformation X axial.
Le conformère X-équatorial est donc plus stable que le conformère X-axial.
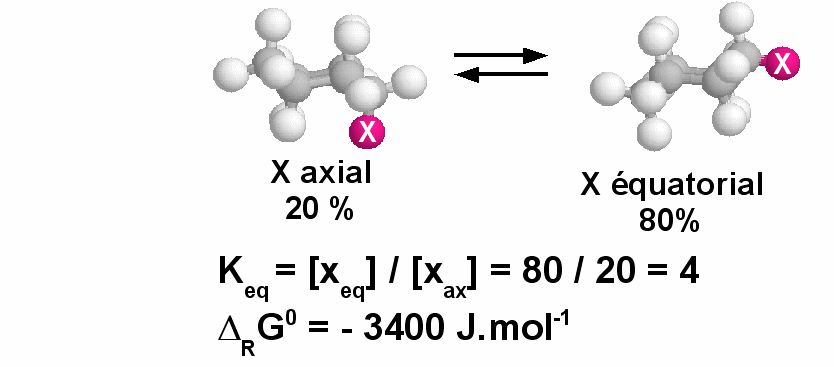
Ces proportions
s'expliquent par les intéractions qui sont différentes
dans les deux conformations.
La conformation X équatorial
présente des interactions beaucoup plus faibles que la
conformation X axial.
|
|
|
|
|
|
|
|
|
|
|
|
Le tableau suivant donne quelques exemples de valeurs expérimentales pour divers substituants pour l'équilibre : : Xaxial = Xéquatorial
|
Substituant |
nom |
DRG0 (kJ.mol-1) |
K |
xeq |
xax |
|
F |
fluoro |
- 1,05 |
1,528 |
0,6 |
0,4 |
|
I |
iodo |
- 1,92 |
2,171 |
0,68 |
0,32 |
|
Cl |
chloro |
- 2,17 |
2,402 |
0,71 |
0,29 |
|
Br |
bromo |
- 2,3 |
2,531 |
0,72 |
0,28 |
|
OCH3 |
éthoxy |
- 3,14 |
3,554 |
0,78 |
0,22 |
|
OH |
hydroxy |
- 3,93 |
4,889 |
0,83 |
0,17 |
|
COO-CH3 |
acétate |
- 5,39 |
8,816 |
0,9 |
0,1 |
|
NH2 |
amino |
- 5,85 |
10,616 |
0,91 |
0,09 |
|
COOH |
Acide carboxylique |
- 5,89 |
10,788 |
0,92 |
0,08 |
|
CH3 |
méthyl |
- 7,11 |
17,657 |
0,95 |
0,05 |
|
CH2CH3 |
éthyl |
- 7,32 |
19,220 |
0,95 |
0,05 |
|
CH(CH3)2 |
isopropyl |
- 9,2 |
41,063 |
0,98 |
0,02 |
|
C(CH3)3 |
tertiobutyl |
- 20,9 |
4627,345 |
1 |
0 |
|
Moyenne |
|
- 3,4 |
4 |
0,80 |
0,2 |
On voit que pour des substituants très encombrants comme isopropyle CH(CH3)2 ou tertio butyle C(CH3)3 la conformation X équatorial est très largement prédominante.
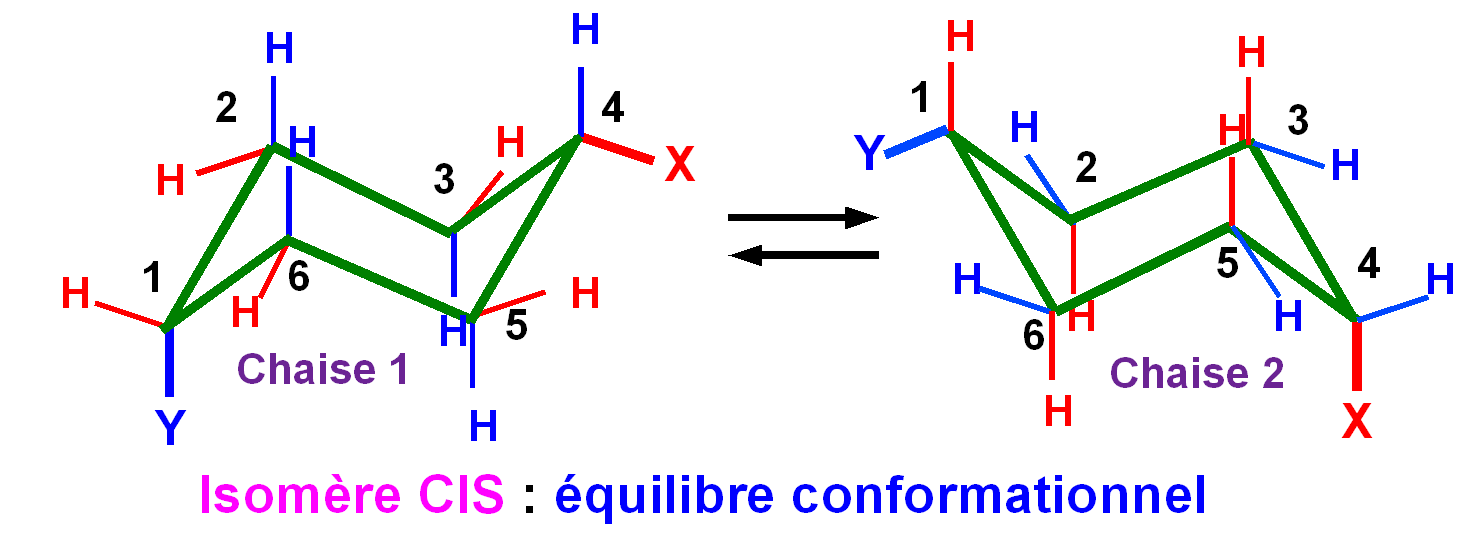
Quand un cyclohexane
présente 2 substituants on observe l'existence de
stéréoisimères différents.
Ce type
d'isomérie est appelé isomérie cis-trans.
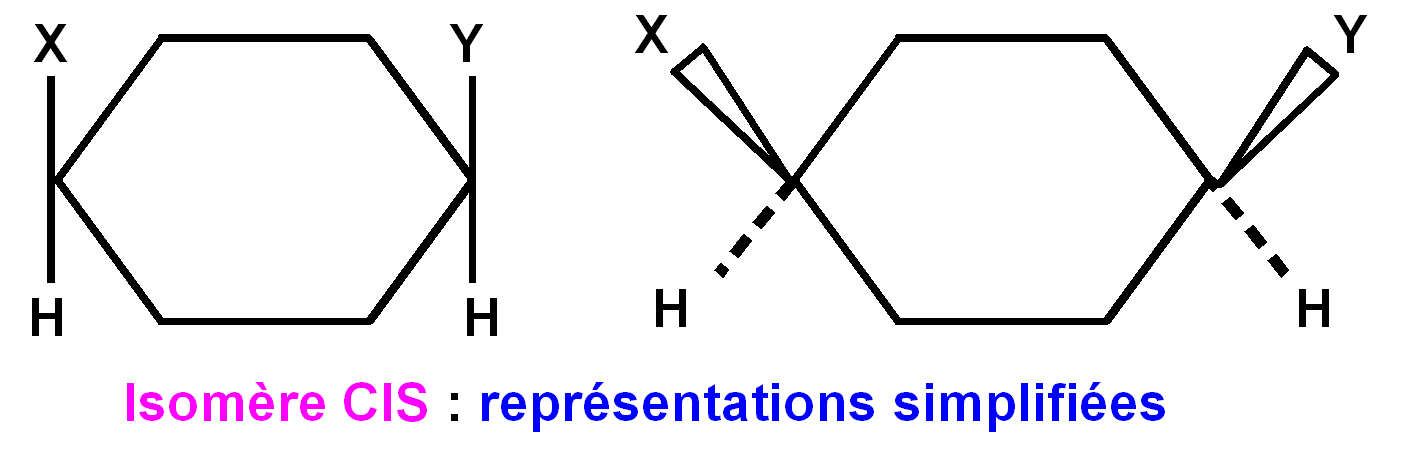
L'isomère cis est celui pour lequel les deux substituants
sont situés du même coté du plan moyen du cycle.
L'isomère trans est celui pour lequel les deux
substituants sont situés de part et d'autre du plan moyen du
cycle.
|
|
|
|
|
|
|
|
|
|
|
|
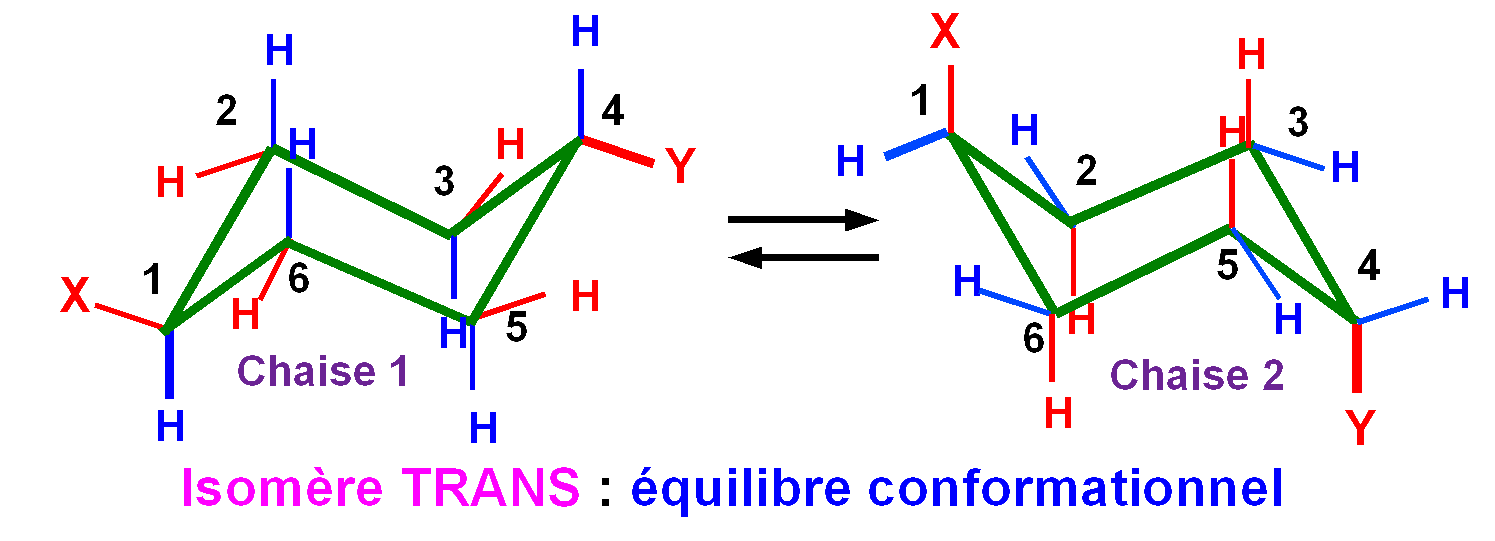
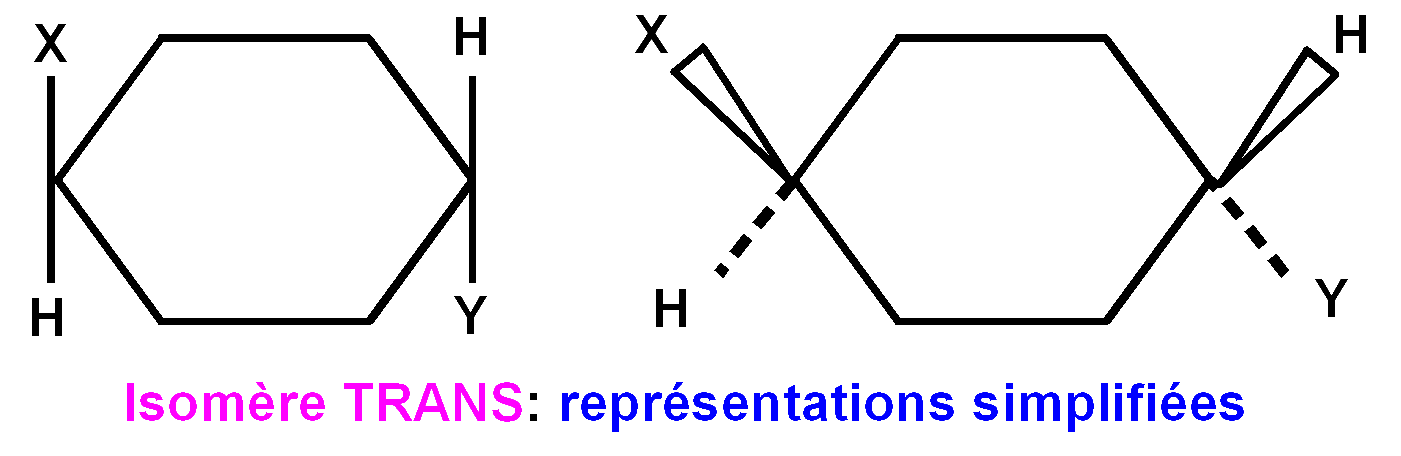
En première approximation, les effets répulsifs des substituants sont sensiblements additifs et on peut utiliser les valeurs des DRG0 relatifs à un substituant pour prévoir ceux relatifs à plusieurs substituants.
Exemple : Méthyl-cyclohexane et diméthyl cyclo hexane
Effet du groupe Méthyl pour l'équilibre : Xaxial = Xéquatorial
|
Substituant |
nom |
DRG0 (kJ.mol-1) |
K |
xeq |
xax |
|
CH3 |
méthyl |
- 7,11 |
17,657 |
0,95 |
0,05 |
Méthyl cyclohexane
L'effet d'un groupement méthyl correspond à un DRG0 = -7,11 kJ.mol-1 en faveur de la conformation équatoriale.
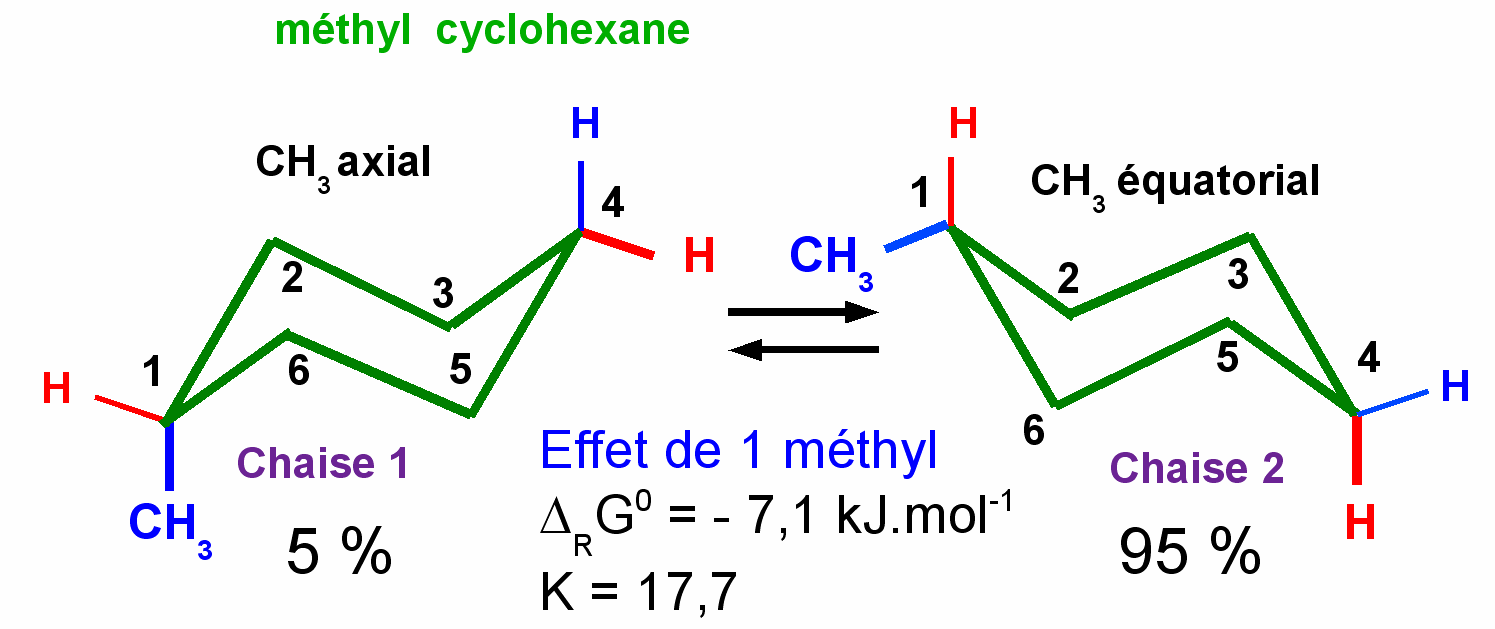
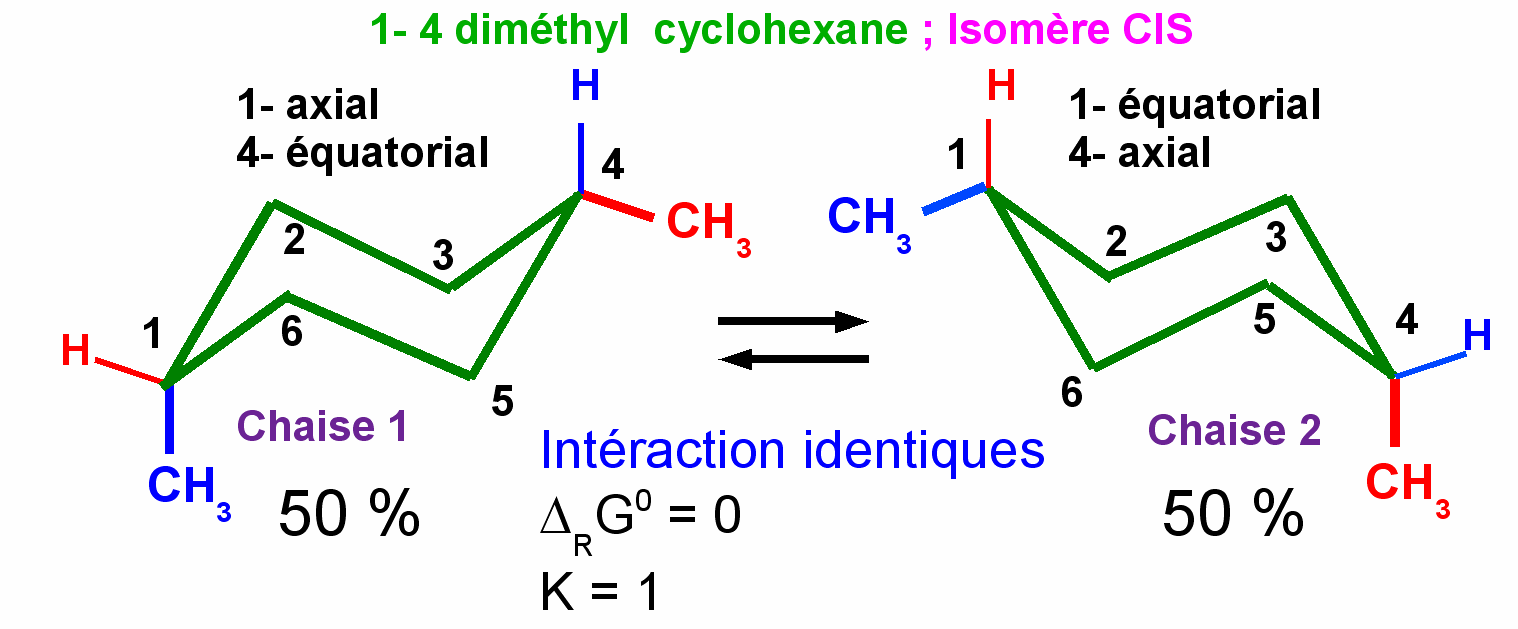
1-4 diméthyl cyclohexane
Pour deux groupes méthyl, l'expérience montre que l'on observe une additivité des effets avec un DRG0 = -14,2 kJ.mol-1 en faveur de la conformation diéquatoriale pour l'isomère trans du 1-4 diméthyl cyclohexane.
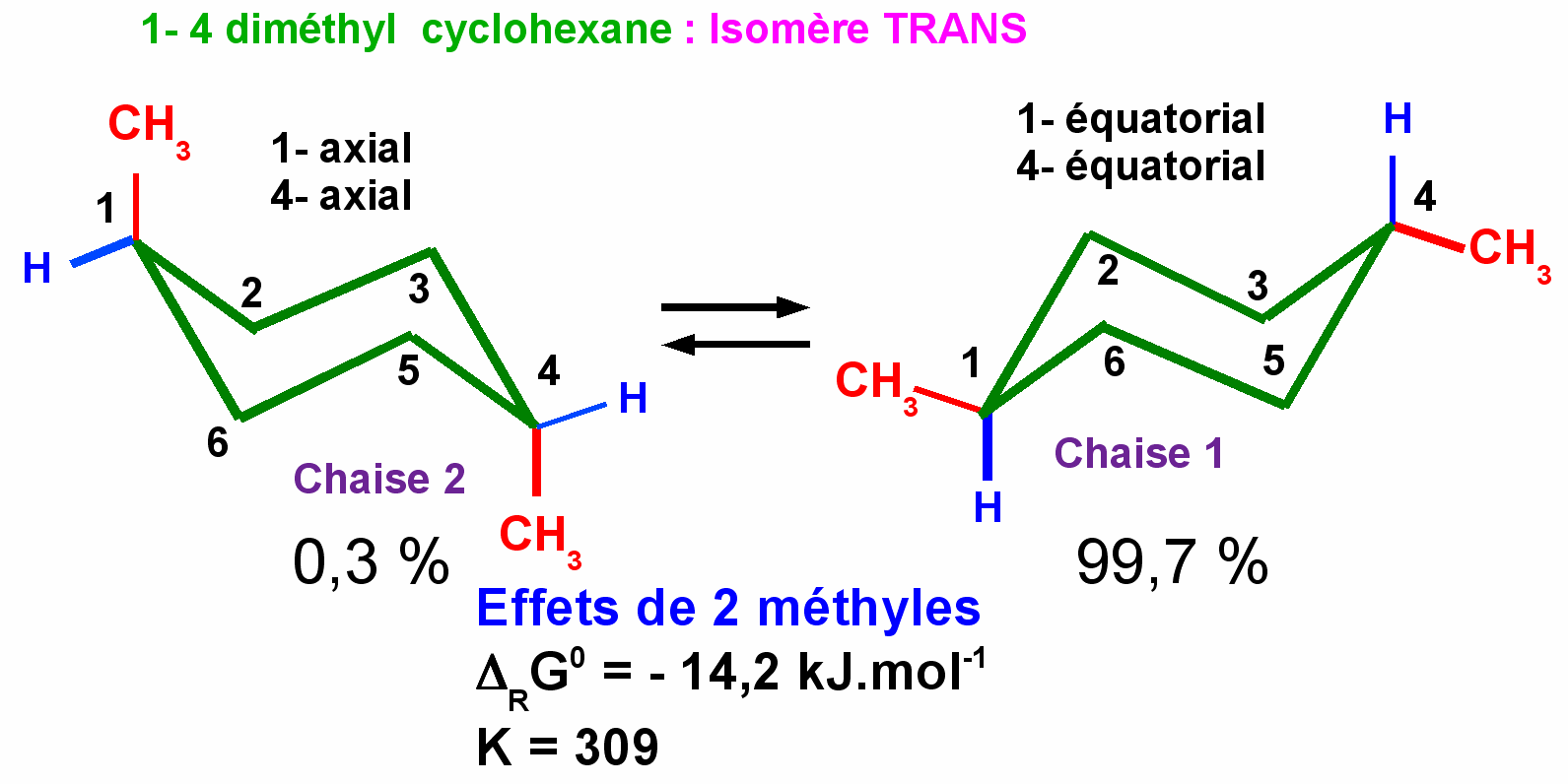
L'isomère cis pour lequel un méthyl est axial et l'autre équatorial ne présentant aucune différence entre ses deux conformations ne sera pas concerné par ces effets et aura donc un DRG0 nul, soit K =1.
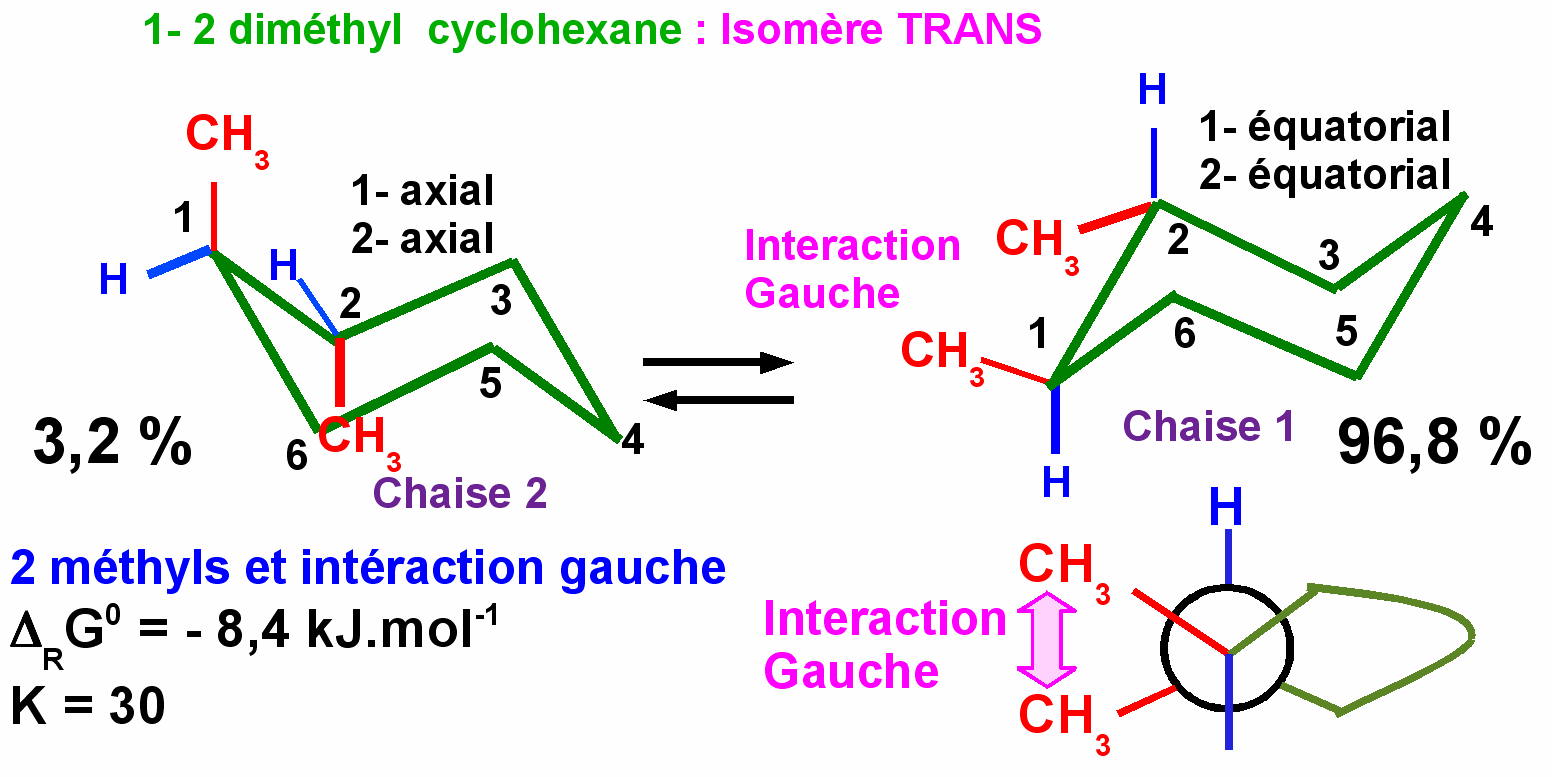
1-2 diméthyl cyclohexane
On pourrait
s'attendre à observer
ici aussi un DRG0
= - 14,2 kJ.mol-1
et K = 309 en faveur de la conformation di-équatoriale.
On
n'observe en fait expérimentalement qu'un DRG0
= -8,4 kJ.mol-1.et
K = 30.
La conformation diéquatoriale est donc moins
favorisée que prévu.
C'est l'interaction gauche entre les deux méthyls équatoriaux qui est responsable de cette diminution de stabilité relative
Règle générale :
Dans
le cas général on constate que les substituants
volumineux se placent préférentiellement en position
équatoriale.
Le conformère le plus stable est donc
généralement celui pour lequel un maximum de
substituants sont en positions équatoriales.