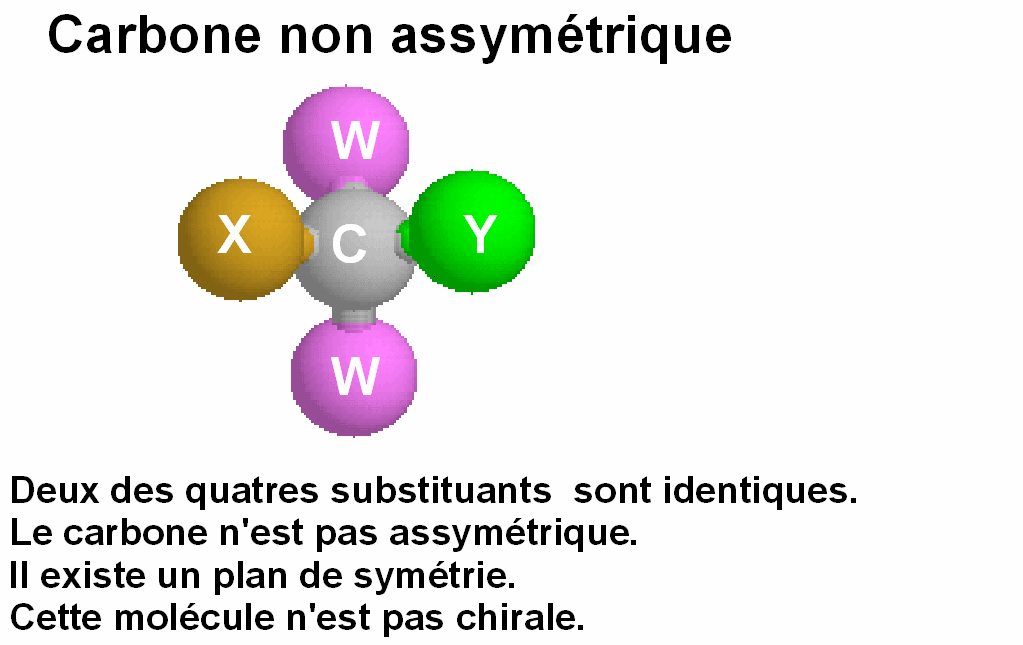
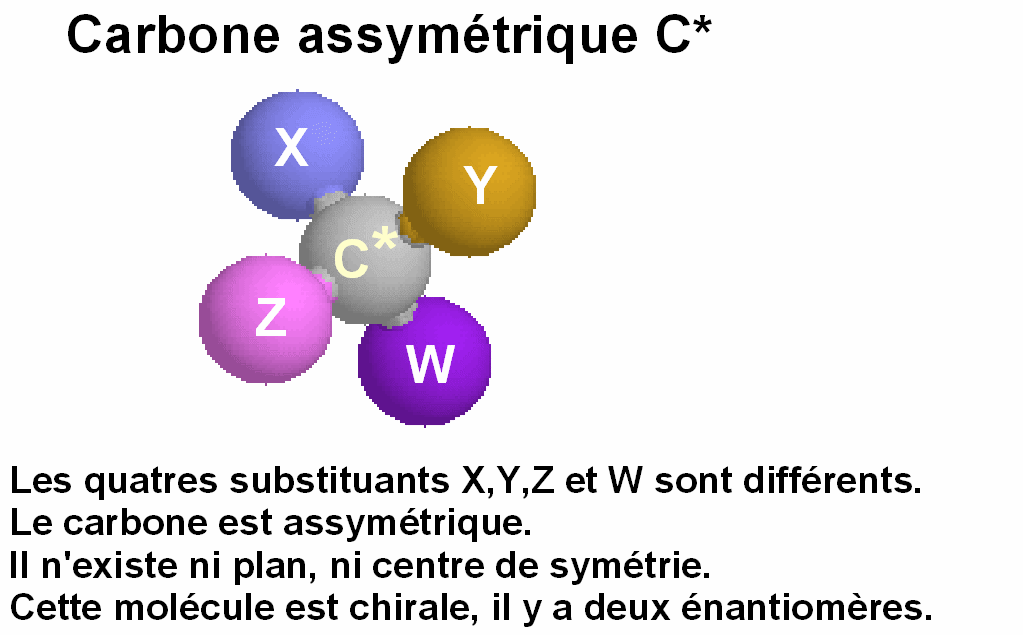
La notion d'énantiomèrie que nous avons définie en introduction est liée à la symétrie moléculaire.
Pour qu'il puisse exister deux énantiomères, il faut que la molécule ne possède ni plan de symétrie, ni centre de symétrie. Quand cela se produit, on dit que la molécule est chirale.
Remarques :
La définition exacte de la chiralité est en fait plus complexe, mais cette définition simple suffira dans cette première approche.
Dans ce cour, nous nous intéresserons uniquement à l’atome de carbone sp3 comme centre de chiralité. D’autre atomes et d’autres structures carbonées sont susceptibles d’être chirales, mais vous approfondirez ces notions ultérieurement.
Le mot chiralité vient du terme grec désignant la main, en effet la main gauche et la main droite constituent un exemple de paires d’énantiomères, elles sont images spéculaires l’une de l’autre et ne sont pas superposables.
Un atome de carbone hybridé sp3 et portant 4 substituants différents (souvent noté C*) est un centre de chiralité qui induit la possibilité d’existence d’énantiomères.
|
|
|
Si une molécule possède un tel
centre, elle pourra être chirale et poura donc exister sous forme d’une paire
d’énantiomères.
Nous verrons que ces deux énantiomères seront désignés par
une notation spécifique indiquant leur configuration absolue l’un sera désigné
comme de configuration R et l’autre comme de configuration S.
Remarques :
Si une molécule possède plusieurs carbones asymétriques elle n’est pas obligatoirement chirale.
En revanche une molécule possédant un seul carbone asymétrique est obligatoirement chirale.
Nous reviendrons en détail sur tout ceci.