SUJET DE CHIMIE THEORIQUE-ATOMISTIQUE
SESSION DE SEPTEMBRE 99 – Deuxième période
LES MOLECULES
LE DIAZOMETHANE
DONNEES :
On rappelle la formule empirique permettant le calcul approché des longueurs de liaisons (en A°) à partir des rayons de covalence calculés des atomes :
Liaison simple : LAB = 1,11 (RA + RB ) - 0,203
Liaison double : 86% de la simple
Liaison triple : 78% de la simple
On donne les rayons de covalence calculés pour C, N et H :
RC = 0,7856 A° - RN = 0,7415 A° - RH = 0,346 A°
Le diazométhane CH2N2 est un composé gazeux très instable (explosif) et très toxique. Il est néanmoins très utilisé en chimie organique pour sa très grande réactivité.
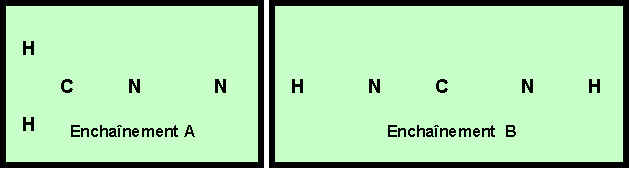
On peut envisager deux enchaînements différents pour cette molécule :

ON SUPPOSERA DANS UN PREMIER TEMPS QUE L'ATOME DE CARBONE NE PORTE PAS DE CHARGES FORMELLES.
2) Pour les deux enchaînement A et B, calculer les longueurs de liaisons prévues.
3) Comparaison avec les longueurs réelles :
Les données expérimentales concernant cette molécule montrent qu’elle est constituée par l’enchaînement de trois types de liaisons de longueurs respectives :
1,08 A°– 1,32 A°– 1,12 A°
| Liaison | Calculée | Expérimentale | Ecart % |
1,08 |
|||
1,12 |
|||
1,32 |
Nota : Ecart % = 100 *( Lcalc - Lexp ) / Lexp
3-5) Intervention de formes mésomères :
Montrer qu'on peut écrire deux autres formes mésomères dans lesquelles l'atome de Carbone porte une charge négative.
4) Pour l’enchaînement B ( H N C N H ) :
4-1) Prévoir la géométrie de la molécule à l’aide de la méthode V.S.E.P.R.
4-2) En déduire l'hybridation des atomes de Carbone et d'Azote dans cette structure B.
4-3 ) Décrire par un schéma la formation des liaisons dans cette structure B.
4-4 ) Montrer que l'on peut déduire du schéma précédant une information supplémentaire sur la géométrie de cet édifice qui ne pouvait être prévue par la méthode V.S.E.P.R