Exercice 1 :
Le butane (gazeux sous 1 bar à 298 K) et l’acétone (liquide sous 1 bar à 298 K) ont des points d’ébullition et des points de fusion très différents bien qu’ils aient tous deux la même masse molaire.
Attribuer à chacun son point d’ébullition et son point d’ébullition.
Justifier les différences observées.
T1 = - 138 °C - T2 = - 0,5 °C - T3 = - 95°C - T4 = + 56°C
Cas du Butane : CH3 - CH2 - CH2 - CH3
Le butane ne présente que des liaisons C -C et C -H.
Les liaisons C - C sont évidemment non polarisées.
Les liaisons C - H le sont très peu car C et H ont des électronégativités très proches.
XC = 2,6 et XH = 2,2 dans l'échelle de Pauling.
Le butane ne présente donc aucune liaisons fortement polarisées et présentera donc peu d'interaction de type Keesom entre moment dipolaires permanents.
Il n'y aura donc pas d'interactions intermoléculaires et le butane aura donc des températures de changement d'état "normales".
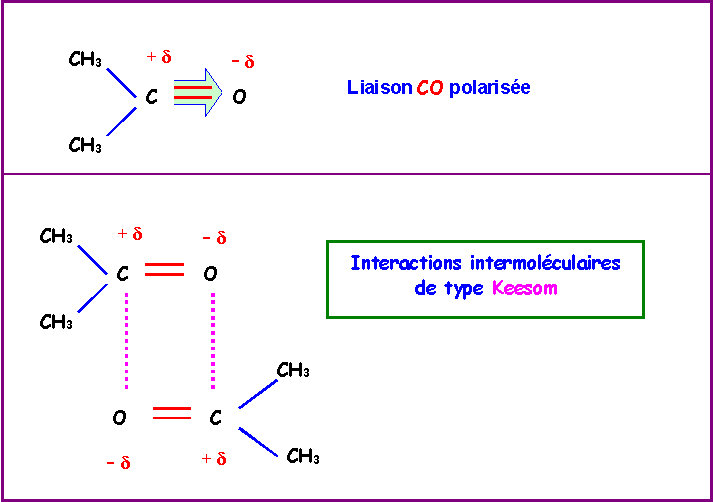
Cas de l'Acétone : CH3 - CO - CH3
En revanche, l'acétone présente une liaisons C = O fortement polarisée ( XO = 3,4 ) et les interaction de Keesom seront donc importantes pour ce composé.
Il y aura donc de fortes interactions intermoléculaires et l'Acétone présentera des températures de changement d'état "anormalement" élevées puisqu'il faudra briser toutes ces "liaisons" intermoléculaires.

L'attribution des températures de changement d'état est donc le suivant :
T1 = -138°C et T3 = -95°C qui sont les deux températures les plus basses sont les deux points de fusion et l'acétone correspond au plus élevé, soit T3.
T2 = -0,5°C et T4 = +56°C qui sont les deux températures les plus élevées sont les deux points d'ébullition et l'acétone correspond au plus élevé, soit T4.
Butane |
Acétone |
|
Point de Fusion |
T1 = - 138 °C |
T3 = - 95°C |
Température d'Ebullition |
T2 = - 0,5 °C |
T4 = + 56°C |