Thierry Briere : www.chimie-briere.com
T.D de Physicochimie des solutions aqueuses
Corrigé des exercices sur les acides et les bases
Exercice 1 :
Calculer le pH des solutions suivantes :
1-1 : Acide chlorhydrique : 0,03 mol.L-1 - 2 10-5 mol.L-1 - 3,2 10-7 mol.L-1 - 10-8 mol.L-1
HCl : acide fort totalement dissocié
* C = 0,03 - pC = 1,52 - pC < 6 è pH = pC = 1,5 (pH exact 1,52)
* C = 2 10-5 - pC = 4,7 - pC < 6 è pH = pC = 4,7 (pH exact 4,699)
* C = 3,2 10-7 - pC = 6,49 - 6 < pC < 7
h = ( C0 + Ö [C02 + 4 Ke] ) / 2 = 3,49 10-7
pH = 6,5 (pH exact 6,457)
* C=10-8 - pC = 8 - pC > 7 -
pH = 7 (pH exact 6,978)
1-2 : Soude : 0,03 mol.L-1 - 2 10-5 mol.L-1 - : 3,2 10-7 mol.L-1
NaOH : base forte totalement dissociée
pOH = pC = 1,52
pH = 12,5 (pH exact 12,48)
pOH = pC = 4,7
pH = 9,3 (pH exact 9,301)
w = ( C0 + Ö [C02 + 4 Ke] ) / 2 = 3,49 10-7
pOH = 6,46
pH = 7,5 (pH exact 7,54)
1-3 : Acide éthanoïque (CH3COOH) : 0,03 mol.L-1 - 2 10-5 mol.L-1 - : 10-6 mol.L-1
Acide éthanoïque : acide faible de pKa = 4,8
pH = 1/2 (pKa + pC ) = 3,2 (pH exact 3,17)
* C = 2 10-5 - pC = 4,7 - pKa - 1 < pC < pKa + 1
h = { -Ka + Ö [ Ka2 + 4 Ka C0 ] } / 2
h = { -10-4,8 + Ö [ 10-9,6 + 4 *10-4,8 * 2 10-5 ] } / 2 = 1,16 10-5
pH = 4,9(pH exact 4,93)
* C = 10-6 - pC = 6 - pC > pKa è pH = pC = 6 (pH exact 6,02)
1-4 : Ethylamine (C2H5NH2) : 0,03 mol.L-1 - 2 10-5 mol.L-1 - : 10-3 mol.L-1
Ethylamine : base faible de pKa = 10,6
pKb = 14 - pKa = 3,4
pOH = 1/2 (pKb + pC ) = 2,46 è pH = 11,5 (pH exact 11,51)
pOH = pC = 4,7
pH = 9,3 (pH exact 9,28)
* C = 10-3 - pC = 3 - pKb - 1 < pC < pKb + 1
w = { -Kb + Ö [ Kb2 + 4 Kb C0 ] } / 2 w = 4,63 10-4
pOH = 3,3
pH = 10,7 (pH exact 10,67)
1-5 : Solution 0,1 mol.L-1 d'acétate d'ammonium (NH4+ CH3COO-)
pKa CH3COO- = 4,8 - pKa NH4+= 9,2
NH4+ = acide faible - CH3COO- = base faible
On a affaire à l'équivalent d'une solution d'ampholyte
pH = 1/2 (pK1 + pK2) = 7 (pH exact 7,000)
1-6 : Solution 0,05 mol.L-1 de carbonate de sodium (Na2CO3)
CO32- dibase faible de pKa : pK1= 6,4 - pK2 = 10,3
Pour simplifier, on ne considère que la première basicité de l'ion carbonate et on néglige donc la deuxième beaucoup plus faible. On considère donc CO32- comme une monobase faible de pKb = 14 - pK2 = 3,7
pC = -log(0,05) = 1,3 - pC < pKb - 1
pOH = 1/2 (pKb + pC ) = 0,5*(3,7+1,3) = 2,5 è pH = 14 - 2,5 = 11,5 (pH exact 11,486)
1-7 : Solution obtenue en dissolvant 0,025 mole d'acétate de sodium (CH3COO-Na+) pKa = 4,8 dans 100 mL d'acide chlorhydrique à 0,25 mol.L-1.
CH3COO- + H3O+ = CH3COOH + H2O
KR = [CH3COOH] / { [CH3COO-] [H3O+] } = 1/Ka = 104,8 (réaction quasi totale)
n CH3COO- = 0,025 mole
n H3O+ = 0,25 * 100 / 1000 = 0,025 mole
On est dans les proportions stoéchiométriques.
CH3COO- |
H3O+ |
CH3COOH |
|
Etat initial |
0,025 |
0,025 |
0 |
Etat final |
0 |
0 |
0,025 |
On est en présence d'une solution d'un acide faible.
C = 0,025 / 100 * 1000 = 0,25 - pC = 0,6 - pC < pKa - 1
pH = 1/2 ( pKa + pC) = 2,7 (pH exact 2,702)
Exercice 2 : Soit une solution A obtenue par dissolution de m g d'éthylamine dans 150 mL d'eau pure. Son pH est de 10,3. Calculer la concentration des diverses espèces présentes en solution et déterminer la valeur de m.
Ethylamine C2H5NH2 : base faible de pKa = 10,6
M = 2*12 + 5 +14 + 2 = 45 g.mol-1
pH = 7 + 1/2 pKa+1/*2 log C = 10,3
7 + 5,3+1/*2 log C = 10,3
7 + 5,3+1/*2 log C = 10,3 è C = 10-4 mol.L-1 è C = 4,5 10-3 g.L-1
m = 4,5 10-3 * 150 / 1000 = 6,75 10-3 g = 6,75 mg
pH = pKa + log { [Base] / [Acide] } = pKa + log R
log R = pH - pKa = 10,3 - 10,6 = -0,3 è R » 0,5
[Base] / [Acide] = 0,5 è [Base] = 0,5 [Acide]
[Base] + [Acide] = C = 10-4
0,5 [Acide] + [Acide] = 10-4 è 1,5 [Acide] = 10-4
[Acide] = 6,67 10-5 mol.L-1
[Base] = 3,33 10-5 mol.L-1
[C2H5NH2] = 3,33 10-5 mol.L-1
[C2H5NH3+] = 6,66 10-5 mol.L-1
[H3O+] = 5 10-11 mol.L-1
[OH-] = 2 10-4 mol.L-1
Exercice 3 :
Soit une solution d'un acide faible BH+ de pKa = 5 évaluer les pourcentages des espèces B et BH+ pour des valeurs de pH de : 1- 2 - 4 - 5 - 6 - 8 - 10
R = [Base] / [Acide] = 10(pH-pKa)
%Acide = 100 / (1 + R )
%Base = 100 R / (1 + R )
pH |
R |
%Acide |
%Base |
1 |
0,0001 |
100,0 |
0,0 |
2 |
0,001 |
99,9 |
0,1 |
4 |
0,1 |
90,9 |
9,1 |
5 |
1 |
50,0 |
50,0 |
6 |
10 |
9,1 |
90,9 |
8 |
1000 |
0,1 |
99,9 |
10 |
100000 |
0,0 |
100,0 |
Exercice 4 :
On mélange 20 mL d'une solution 0,2 mol.L-1 d'acide chlorhydrique et 50 mL d'une solution 0,25 mol.L-1 d'ammoniaque.
NH3 + H3O+ = NH4+ + H2O
KR = [NH4+] / { [NH3] [H3O+] } = 1 / Ka = 109,25 (réaction quasi totale)
Etat initial
nHCl = 20 * 0,2 / 1000 = 4 10-3 mole (défaut)
nNH3 = 50 * 0,25 / 1000 = 12,5 10-3 mole (excès)
Etat final :
nNH3 = 12,5 10-3 - 4 10-3 = 8,5 10-3 mole è [NH3] = 8,5 / 70 = 0,121 mol.L-1
nNH4+ = 4 10-3 mole è [NH4+] = 4 / 70 = 0,0571 mol.L-1
R = [Base] / [Acide] = [NH3] / [NH4+] = 2,125 è log R = 0,327
pH = pKa + log R = 9,6 (pH exact 9,57)
Exercice 5 :
Soit une solution A obtenue par dissolution de 0,75 mole de chlorure d'éthylammonium (EtNH3+Cl- - pKa=10,6) dans 1 litre de solution de soude (Na+OH-) à 0,25 mol.L-1.
EtNH3+ + OH- = EtNH2 + H2O
KR = { [EtNH2] / [EtNH3+] [OH-] } = 1 / Kb = 103,4 (réaction quasi totale)
Etat initial
nNaOH= 0,25 (défaut)
nEtNH3+ = 0,75 mole (excès)
Etat final :
nEtNH3+ = 0,75 - 0,25 = 0,5 mole è [EtNH2] = 0,5 mol.L-1
nEtNH2 = 0,25 mole è [RNH3+] = 0,25 mol.L-1
R = [Base] / [Acide] = [EtNH2] / [EtNH3+] = 0,5 è log R = -0,3
pH = pKa + log R = 10,3
(la résolution exacte donne pH = 10,299)
Résolution approximative :
EtNH2 + H3O+ = EtNH3+ + H2O
KR = { [EtNH3+] / ( [EtNH2] [H3O+] ) } = 1 / Ka = 1010,6 (réaction quasi totale)
On ajoute HCl (Va), cela ne modifie pas le nombre de mole total (sous deux formes) de l'espèce [ EtNH2 - EtNH3+ ]. En revanche le rapport R est modifié.
pH = pKa + log R = 10
log R = pH - pKa + = 10 - 10,6 = -0,6 è R = 0,25
De plus le pH étant basique on sait que HCl est en défaut.
| EtNH2 | H3O+ | EtNH3+ | |
| Etat initial | 100*0,25/1000 = 0,025 | x | 100*0,5/1000 = 0,05 |
| Etat final | 0,025 - x | 0 | 0,05 + x |
R = 0,25 = ( 0,025 - x ) / ( 0,05 + x )
Remarque : Le volume total se simplifie
x = 0,01 mole de HCl molaire soit Va = 0,01 L = 10 mL
Résolution exacte :
Rappel de l'énoncé : Soit une solution A obtenue par dissolution de 0,75 mole de chlorure d'éthylammonium (EtNH3+ - pKa=10,6) dans 1 litre de solution de soude (Na+OH-) à 0,25 mol.L-1. Quel volume de solution molaire de HCl faut-il ajouter à 100 mL de cette solution A pour que son pH passe à 10 ?
Espèces présentes : EtNH3+ - EtNH2 - Cl- - Na+ - H3O+ - OH-
pH = 10
[H3O+] = h = 10-10 mol.L-1
[OH-] = w = Ke / h = 10-4 mol.L-1
R = 10(pH-pKa) = 10(10-10,6) = 0,2512
C0 EtNH3+Cl- = 0,75 * 100 / (100 + V ) = 75 / ( 100 + V )
[EtNH3+] = C0 / ( 1 + R ) = 75 / ( 100 + V ) / 1,2512 = 59,943 / ( 100 + V )
[Cl-] = ( 0,75 * 100 + 1*V ) / ( 100 + V ) = (75 + V) / ( 100 + V )
[Na+] = 100 * 0,25 / ( 100 + V ) = 25 / ( 100 + V )
E.N : [EtNH3+] + [H3O+] + [Na+] = [Cl-] + [OH-]
[EtNH3+] + [Na+] - [Cl-] = [OH-] - [H3O+] = 9,99999 10-5
59,943 / ( 100 + V ) + 25 / ( 100 + V ) - (75 + V) / ( 100 + V ) = 9,99999 10-5
59,943 + 25 - 75 - V = 9,99999 10-5 ( 100 + V )
9,943 - V = 9,99999 10-3 + 9,99999 10-5 V
9,943 - 9,99999 10-3 = ( 1 + 9,99999 10-5 ) V
V = 9,93 mL
La résolution approximative est bonne à 0,7 % près et est donc acceptable.
Résolution approchée :
EtNH3+ + OH- = EtNH2+ H2O
KR = { [EtNH2] / ([EtNH3+] [OH-] ) } = 1 / Kb = 103,4 (réaction quasi totale)
On ajoute NaOH (Vb), cela ne modifie pas le nombre de mole total (sous deux formes) de l'espèce [ EtNH2 - EtNH3+ ]. En revanche le rapport R est modifié.
pH = pKa + log R = 11,2
log R = pH - pKa + = 11,2 - 10,6 = 0,6 è R = 4
De plus le pH étant basique on sait que HCl est en défaut.
| EtNH3+ | OH- | EtNH2 | |
| Etat initial | 100*0,5/1000 = 0,05 | x | 100*0,25/1000 = 0,025 |
| Etat final | 0,05 - x | 0 | 0,025 + x |
R = 4 = ( 0,025 + x ) / ( 0,05 - x )
Remarque : Le volume total se simplifie
x = 0,035 mole de NaOH molaire soit Vb = 0,035 L = 35 mL
Résolution exacte :
Rappel de l'énoncé : Soit une solution A obtenue par dissolution de 0,75 mole de chlorure d'éthylammonium (EtNH3+ - pKa=10,6) dans 1 litre de solution de soude (Na+OH-) à 0,25 mol.L-1. Quel volume de solution molaire de soude faut-il ajouter à 100 mL de cette solution A pour que son pH passe à 11,2 ?
Espèces présentes : EtNH3+ - EtNH2 - Cl- - Na+ - H3O+ - OH-
pH = 11,2
[H3O+] = h = 10-11,2 = 6,3096 10-12 mol.L-1
[OH-] = w = Ke / h = 1,5849 10-3 mol.L-1
R = 10(pH-pKa) = 10(11,2-10,6) = 3,9811
C0 EtNH3+Cl- = 0,75 * 100 / (100 + V ) = 75 / ( 100 + V )
[EtNH3+] = C0 / ( 1 + R ) = 75 / ( 100 + V ) / 4,9811 = 15,057 / ( 100 + V )
[Cl-] = C0 = 75 / ( 100 + V )
[Na+] = (100 * 0,25 + 1* V ) / ( 100 + V ) = ( 25 + V )/ ( 100 + V )
E.N : [EtNH3+] + [H3O+] + [Na+] = [Cl-] + [OH-]
[EtNH3+] + [Na+] - [Cl-] = [OH-] - [H3O+] = 9,99999 10-5
15,057 / ( 100 + V ) + ( 25 + V ) / ( 100 + V ) - 75 / ( 100 + V )= 1,5849 10-3
15,057 + 25 + V - 75 = 1,5849 10-3 ( 100 + V )
15,057 + 25 + V - 75 = 1,5849 10-3 ( 100 + V )
-34,943 + V = 1,5849 10-1 + 1,5849 10-3 V
V - 1,5849 10-3 V = 1,5849 10-1 + 34,943
V (1 - 1,5849 10-3) = 1,5849 10-1 + 34,943
V = (1,5849 10-1 + 34,943) /(1 - 1,5849 10-3)
V = 35,15 mL
La résolution approximative est bonne à 0,43 % près et est donc tout a fait acceptable.
pH = 11,2
[H3O+] = 10-11,2 = 6,3 10-12 mol.L-1
[OH-] = 0,001585 mol.L-1
R = 4
C = 0,075 * 1000 / 135 = 0,555 mol.L-1
[EtNH3+] = 0,555 / 5 = 0,111 mol.L-1
[EtNH2] = 4 * 0,111 = 0,444 mol.L-1
On peut aussi utiliser la valeur de x trouvée pour accéder directement aux concentrations cherchées.
[EtNH3+] = (0,05 - x) / V = (0,05 - 0,035) / 135 10-3 = 0,111 mol.L-1
[EtNH2] = (0,025 + x) / V = (0,025 - 0,035) / 135 10-3 = 0,444 mol.L-1
Exercice 6
On titre 20 mL d'une solution à 0,05 mol.L-1 d'une base faible de pKa = 7,5 par un acide fort de molarité 0,1 mol.L-1.
Calculer le pH pour les volumes suivant d'acide versé :
V = 0 mL - 2 mL - 4 mL - 5 mL - 6 mL - 8 mL - 10 mL -12 mL - 14 mL - 16 mL - 18 mL
Tracer la courbe de titrage
Quel indicateur coloré convient le mieux pour ce titrage ?
Hélianthine (3,1-4,4) - B.B.T (6,2-7,6) - Phénolphtaléine (8-10)
B + H3O+ = BH+ + H2O
KR = [BH+] / { [B] [H3O+] } = 1 / Ka = 107,5 (réaction quasi totale)
Détermination de Veq
CaVa = CbVb è Va = CbVb/Ca = 0,05*20/0,1 = 10 mL
* Pour V = 0 : Solution de base faible pKa = 7,5 è pKb = 14 - 7,5 = 6,5
pC = -log 0,05 = 1,3 - pC < pKb - 1 è pH = 1/2 ( pKb + pC ) = 10,1
* Pour V < 10 mL : Base faible en excès - Acide fort en défaut
B + H3O+ = BH+ + H2O
B |
H3O+ |
BH+ |
|
Etat initial |
Cb Vb |
Ca Va |
0 |
Etat final |
Cb Vb - Ca Va |
0 |
CaVa |
pH = pKa + log R = pKa + log { ( Cb Vb - CaVa ) / Ca Va ) }
pH = 7,5 + log { ( 1 - 0,1Va ) / 0,1 Va ) }
Remarque : le volume total se simplifie
Va |
2 |
4 |
5 |
6 |
8 |
pH |
8,1 |
7,7 |
7,5 |
7,3 |
6,9 |
pH exact |
8,102 |
7,676 |
7,500 |
7,324 |
6,897 |
* Pour V > 10 mL : Base faible en défaut - Acide fort en excès
B + H3O+ = BH+ + H2O
B |
H3O+ |
BH+ |
|
Etat initial |
Cb Vb |
Ca Va |
0 |
Etat final |
0 |
Ca Va - Cb Vb |
CbVb |
On est en présence d'unb mélange de deux acides, l'acide le plus fort fixe le pH
pH = -log { (CaVa - Cb Vb) / ( Va + Vb ) } = -log { (0,1 Va - 1)/(20+ Va) }
Va |
12 |
14 |
15 |
16 |
18 |
pH |
2,2 |
1,9 |
1,85 |
1,8 |
1,7 |
pH exact |
2,204 |
1,929 |
1,845 |
1,778 |
1,677 |
B + H3O+ = BH+ + H2O
B |
H3O+ |
BH+ |
|
Etat initial |
Cb Vb |
Ca Va = Cb Vb |
0 |
Etat final |
0 |
0 |
CbVb |
On est en présence d'une solution d'acide faible
C = Cb Vb / ( Va + Vb ) = 0,05 * 20 / 30 = 0,0333 - pC = 1,48 - pC < pka - 1
pH = 1/2 ( pKa + pC ) = 4,5
(pH exact = 4,489)
L'indicateur convenable est l'hélianthine
Exercice 7
On titre 10 mL d'une solution à 0,025 mol.L-1 d'un acide faible de pKa = 5,8 par une base forte de molarité 0,05 mol.L-1.
Déterminer le volume de base à verser pour obtenir l'équivalence.
Calculer le pH pour les volumes suivant d'acide versé :
V = 0 - V = 1 mL - V = 2,5 mL - V = 5 mL - V = 6 mL- V = 7,5 mL - V=10 mL
Tracer l'allure de la courbe de titrage
Quel indicateur coloré convient le mieux pour ce titrage ?
Hélianthine (3,1-4,4) - B.B.T (6,2-7,6) - Phénolphtaléine (8-10)
pKa = 5,8 è pKb = 14 - 5,8 = 8,2
BH+ + OH- = B + H2O
KR = [B] / {[BH+] [OH-] } = 1 / Kb = 108,2 (réaction quasi totale)
Détermination de Veq
CaVa = CbVb è Vb = CaVa/Cb = 0,025*10/0,05 = 5 mL
Pour V = 0 : Solution d'acide faible pKa = 5,8
pC = -log 0,025 = 1,6 - pC < pKa - 1 è pH = 1/2 ( pKa + pC ) = 3,7
* Pour V < 5 mL : Acidefaible en excès - Base forte en défaut
BH+ + OH- = B + H2O
BH+ |
OH- |
B |
|
Etat initial |
Ca Va |
Cb Vb |
0 |
Etat final |
Ca Va - Cb Vb |
0 |
CbVb |
pH = pKa + log R = pKa + log { Cb Vb / (Ca Va - CbVb ) }
pH = 5,8 + log { 0,05 Vb / ( 0,25 - 0,05Vb ) }
Remarque : le volume total se simplifie
Va |
1 |
2,5 |
pH |
5,2 |
5,8 |
pH exact |
5,199 |
5,7999 |
BH+ + OH- = B + H2O
BH+ |
OH- |
B |
|
Etat initial |
Ca Va |
Cb Vb |
0 |
Etat final |
0 |
Cb Vb - Ca Va |
CaVa |
On est en présence d'un mélange de deux bases, la base la plus forte fixe le pH
pOH = -log { (CbVb - Ca Va) / ( Va + Vb ) } = -log { (0,05 Vb - 0,25) /(10 + Vb) }
pH = 14 - pOH
Va |
6 |
7,5 |
10 |
pH |
11,5 |
11,85 |
12,1 |
pH exact |
11,495 |
11,854 |
12,097 |
BH+ + OH- = B + H2O
BH+ |
OH- |
B |
|
Etat initial |
Ca Va |
Ca Va = Cb Vb |
0 |
Etat final |
0 |
0 |
CbVb |
On est en présence d'une solution de base faible de pKb = 8,2
C = Cb Vb / ( Va + Vb ) = 0,05 * 5 / 15 = 0,0167 - pC = 1,78 - pC < pkb - 1
pOH = 1/2 ( pKb + pC ) = 5 et pH = 14 - pOH = 9 (pH exact 8,999)
La phénolphtaléïne convient pour ce titrage.

Exercice 8 :
La thréonine est un acide aminé caractérisé par les valeurs suivantes de pKa : pK1=2,6 - pK2=10,6 . Sa formule semi-développée est la suivante :
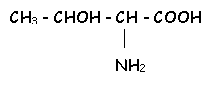
Formule du zwiterion
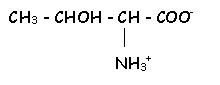
Diagramme de prédominance
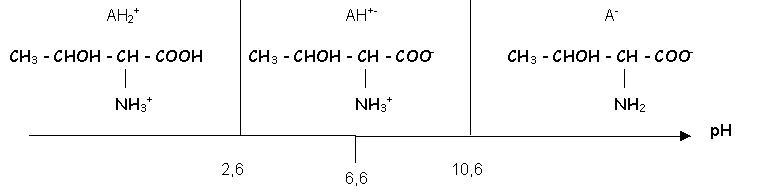
Le switérion est un ampholythe. pH = 1/2 (pK1 + pK2) = 6,6
Résolution exacte :
pH = 2,6
[H3O+] = 10-2,6 = 2,512 10-3 mol.L-1
[OH-] = 10-14/[H3O+] = 3,981 10-12 mol.L-1
[OH-] est ultra minoritaire à ce pH et pourra donc être négligé par la suite.
pH = pK1 + log [AH+-] / [AH2+]
log [AH+-] / [AH2+] = pH - pK1
R1 = [AH+-] / [AH2+] = 10(pH - pK1) = 10(2,6-2,6) = 1
[AH+-] = [AH2+]
pH = pK2 + log [A-] / [AH+-]
log [A-] / [AH+-] = pH - pK2
R2 = [A-] / [AH+-] = 10(pH - pK2) = 10(2,6-10,6) = 10-8
[A-] = 10-8 [AH+-] = 10-8 [AH2+]
[A-] est ultra minoritaire à ce pH et pourra donc être négligé par la suite.
C.M(A) : [A-] + [AH+-] + [AH2+] = C1 = 100*0,1/(100+V) = 10/(100+V)
10-8 [AH2+] + [AH2+] + [AH2+] = 10/(100+V)
[AH2+] ( 2 + 10-8) = 10 / (100+V)
[AH2+] = [AH+-] = 5 / (100+V)
C.M(Cl) : [Cl-] = C2 = 0,1 * V / (100+V)
E.N : [A-] + [OH-] + [AH+-] + [Cl-] = [AH2+] + [H3O+] + [AH+-]
[A-] + [OH-] + [Cl-] = [AH2+] + [H3O+]
[Cl-] - [AH2+] = [H3O+] = 2,512 10-3
0,1 * V / (100+V) - 5 / (100+V) = 2,512 10-3
0,1 * V - 5 = 2,512 10-3 (100+V)
0,1 * V - 5 = 0,2512 + 2,512 10-3 V
0,1 * V - 2,512 10-3 V = 5,2512
V (0,1 - 2,512 10-3) = 5,2512
V = 5,2512 / (0,1 - 2,512 10-3) = 53,87 mL
On trouve donc V = 53,9 mL
L'approximation (Va = 50 mL) n'est donc pas très bonne, cela est principalement dû à la relativement faible valeur de KR, la réaction n'est pas vraiment totale.
A ce pH les deux formes largement majoritaires (en proportions égales puisque pH = pK1) sont AH2+ et AH+-.
* Quel volume de soude 0,20 mol.L-1 faut-il ajouter à 150 mL de solution A pour obtenir un pH de 10,6 ?
AH+- + OH- = A- + H2O
KR = [A-] / { [AH+-] [OH-] } = 1/Kb2 = 103,4
Supposons pour simplifier que la réaction soit quasi totale.
On veut que pH = pK2, on doit donc être à la demi neutralisation de AH+-
Volume de neutralisation : Ca Va = Cb Vb è Vb = Ca Va / Cb = 75 mL
On doit donc ajouter environ 37,5 mL de NaOH au 150 mL de la solution initiale pour obtenir pH=10,6.
On peut aussi faire une résolution exacte.
Résolution exacte :
pH = 10,6
[H3O+] = 10-10,6 = 2,512 10-11 mol.L-1
[OH-] = 10-14/[H3O+] = 3,981 10-4 mol.L-1
[H3O+] est ultra minoritaire à ce pH et pourra donc être négligé par la suite.
pH = pK1 + log [AH+-] / [AH2+]
log [AH+-] / [AH2+] = pH - pK1
R1 = [AH+-] / [AH2+] = 10(pH - pK1) = 10(10,6-2,6) = 108
[AH+-] = 108 [AH2+]
[AH2+]= 10-8 [AH+-]
[AH2+] est ultra minoritaire à ce pH et pourra donc être négligé par la suite.
pH = pK2 + log [A-] / [AH+-]
log [A-] / [AH+-] = pH - pK2
R2 = [A-] / [AH+-] = 10(pH - pK2) = 10(10,6-10,6) = 1
[A-] = [AH+-]
C.M(A) : [A-] + [AH+-] + [AH2+] = C1 = 150*0,1/(100+V) = 15/(150+V)
[AH+-] + [AH+-] + 10-8 [AH+-] = 15/(150+V)
[AH+-] ( 2 + 10-8) = 15 / (150+V)
[A-] = [AH+-] = 7,5 / (150+V)
C.M(Na) : [Na+] = C2 = 0,2 * V / (150+V)
E.N : [A-] + [OH-] + [AH+-] = [AH2+] + [H3O+] + [AH+-]+ [Na+]
[A-] + [OH-] = [AH2+] + [H3O+] + [Na+]
[A-] + [OH-] = [Na+]
[Na+] - [A-] = [OH-]
0,2 * V / (150+V) - 7,5 / (150+V) = 3,981 10-4
0,2 * V - 7,5 = 3,981 10-4 (150+V)
0,2 * V - 7,5 = 0,05972 + 3,981 10-4 V
0,2 * V - 3,981 10-4 V = 0,05972 + 7,5
(0,2 - 3,981 10-4 )V = 0,05972 + 7,5
0,1996 V = 7,55972
V = 7,55972 / 0,1996
V = 37,87 mL
On trouve V=37,9 mL
Le calcul approximatif (Va=37,5 mL) est donc bien meilleur que dans le cas précédant, cela est du principalement à la plus grande valeur de KR.
On se contente très souvent d'un calcul approximatif dans ce genre de problèmes mais puisque la résolution exacte n'est pas très compliquée pourquoi s'en priver si on en a le temps ?
A ce pH les deux formes largement majoritaires (en proportions égales puisque pH = pK2) sont A- et AH+-.
Exercice 9 :
On veut préparer 500 mL d'une solution tampon A de pH=8,5 pour cela on utilise une solution B de base forte à 0,25 mol.L-1 et une solution C d'un acide faible (pKa=9) à 0,2 mol.L-1. Quels volumes de solutions B et C doit-on mélanger ?
Résolution approximative :
AH + OH- = A- + H2O
KR = [A-] / { [AH] [OH-] } = 1 / Ka = 109,25
KR = [A-] [H3O+] / { [AH] [OH-] [H3O+] }
KR = { [A-] [H3O+] / [AH] } / { [OH-] [H3O+] } = Ka / Ke = 105(réaction quasi totale)
Puisque on veut avoir une solution tampon AH est obligatoiremernt en excès.
AH |
OH- |
A- |
|
Etat initial |
Ca Va |
Cb Vb |
0 |
Etat Final |
Ca Va - Cb Vb |
0 |
Cb Vb |
R = [A-] / [AH]
R = Cb Vb / (Ca Va - Cb Vb )
R (Ca Va - Cb Vb )= Cb Vb
R Ca Va - R Cb Vb = Cb Vb
R Ca Va = Cb Vb + R Cb Vb = Cb Vb ( 1 + R )
Va = (Cb / Ca) { ( 1 + R ) / R } Vb
Posons Cb / Ca = O et (1+R) / R = X
Va = XO Vb
Va + Vb = Vt
XOVb + Vb = Vt
Vb = Vt / (1+XO)
pH = pKa + log R è R = 10(pH-pKa)
Application numérique :
R = 10(8,5-9) = 10-0,5 = 0,316
X = (1+R) / R = 1,316/0,316 = 4,165
O = Cb / Ca = 0,25 / 0,2 = 1,25
XO = 4,165*1,25 = 5,21
Vb = Vt / (1+XO) = 500 / 6,21 = 80,5 mL
Va = 500 - 80.5 = 419,5 mL
Résolution exacte :
pH = 8,5
R = 10(pH-pKa) = 10(8,5-9) = 10-0,5 = 0,3162
[AH] = C / ( 1 + R ) = C / 1,3162 = 0,75975 C
[A-] = R C / ( 1 + R ) = 0,24025 C
C = 0,2 Va / 500 = 4 10-4 Va
[AH] = 0,75975 C = 3,039 10-4 Va
[A-] = 0,24025 C = 9,6101 10-5 Va
[H3O+] = 10-8,5 = 3,1623 10-9
[OH-] = Ke/[H3O+] = 3,1623 10-6
C.M(Na) : [Na+] = 0,25 Vb / 500 = 5 10-4 Vb
E.N : [OH-] + [A-] = [H3O+] + [Na+]
[OH-] - [H3O+] = [Na+] - [A-]
3,1591 10-6 = 5 10-4 Vb - 9,6101 10-5 Va
Va + Vb = 500
Va = 500 - Vb
3,1591 10-6 = 5 10-4 Vb - 9,6101 10-5 (500-Vb)
3,1591 10-6 = 5 10-4 Vb - 9,6101 10-5 *500 + 9,6101 10-5 Vb
3,1591 10-6 = 5,961 10-4 Vb - 0,04805
5,961 10-4 Vb = 3,1591 10-6 + 0,04805
5,961 10-4 Vb = 0,048053
Vb = 0,048053 / 5,961 10-4 = 80,6 mL
Va = 500 - 80,61 = 419,4 mL
On trouve VAH = 80,6 mL et VNaOH = 419,4 mL. La résolution approximative était donc tout à fait satisfaisante.
Exercice 10 :
L'acide succinique est un diacide de formule COOH-CH2-CH2-COOH caractérisé par pK1=4,2 et pK2=5,6.
1) Quel est le pH d'une solution 0,2 mol.L-1 de cet acide ?
2) Calculer les concentrations des espèces présentes en solution.
3) A l'aide de cette solution et d'une solution de soude à 2 mol.L-1, on veut préparer 500 mL de solution tampon de pH = 6. Quelles quantités des deux solutions faut-il mélanger ?
1) Quel est le pH d'une solution 0,2 mol.L-1 de cet acide ?
On considère uniquement la première acidité et on néglige donc la deuxième beaucoup plus faible. On considère donc simplement qu'il s'agit d'un monoacide faible de pKa = 4,2.
pC = -log 0,2 = 0,698
pC < pKa - 1 è pH = 1/2 ( pKa+pC )
pH = 2,45
(le pH calculé sans approximation est de 2,453)
2) Calculer les concentrations des espèces présentes en solution.
R1 = 10(pH-pK1) = 0,0178
R2 = 10(pH-pK2) = 7,08 10-4
[AH2] = C / ( 1 + R1 + R1R2) = 0,1965 mol.L-1
[AH-] = C R1 / ( 1 + R1 + R1R2) = 0,00349 mol.L-1
[A2-] = C R1 R2 / ( 1 + R1 + R1R2) = 2,47 10-6 mol.L-1
[H3O+] = 10-pH = 0,0035 mol.L-1
[OH-] = 2,82 10-12 mol.L-1
Remarque : On retrouve le fait que la deuxième acidité est bien négligeable puisque A2- est très peu présent en solution.
3) A l'aide de cette solution et d'une solution de soude à 2 mol.L-1, on veut préparer 500 mL de solution tampon de pH = 6. Quelles quantités des deux solutions faut-il mélanger ?
Résolution approximative :
Appelons Va le volume de solution d'acide succinique et Vb le volume de solution de soude qu'il faut mélanger pour obtenir les 500 mL de tampon de pH = 6.
On a : (1) : Va + Vb = 500
pK1 = 4,2 - pK2 = 5,6 - pH = 6
pH > pK2
On voit qu'il faut neutraliser totalement la première acidité et une partie de la deuxième. Il se produit les deux réactions suivantes
R1 : AH2 + OH- = AH- + H2O :
KR1 = [AH-] / { [AH2] [OH-] } = 1/Kb2 = 108,4 (réaction quasi totale)
R2 : AH- + OH- = A2- + H2O
KR2 = [A2-] / { [AH-] [OH-] } = 1/Kb1 = 109,8(réaction quasi totale)
Appelons V1 le volume de soude nécessaire pour neutraliser la première acidité et V2 le volume suplémentaire correspondant a la neutralisation partielle de la deuxième acidité.
On a (2) : Vb = V1 + V2
Volume de soude nécessaire pour neutraliser une acidité :
V1 = Ca Va / Cb = 0,2 Va / 2 = 0,1 Va
(2) devient : Vb = 0,1 Va + V2
Neutralisation complète de la première acidité :
R1 : AH2 + OH- = AH- + H2O
AH2 |
OH- |
AH- |
|
Etat initial |
Ca Va |
Cb V1 |
0 |
Etat final |
0 |
0 |
Cb V1 |
Neutralisation partielle de la deuxième acidité :
R1 : AH- + OH- = A2- + H2O
AH- |
OH- |
A2- |
|
Etat initial |
Cb V1 |
Cb V2 |
0 |
Etat final |
Cb V1 - Cb V2 |
0 |
Cb V2 |
On a : pH = pK2 + log { [A2-] / [AH-] } = pK2 + log R2
Soit R2 = 10(pH-pK2) = 10(6-5,.6) = 100,4 = 2,512
R2 = 2,512 = { [A2-] / [AH-] } = Cb V2 / { Cb V1 - Cb V2 } = V2 / ( V1 - V2)
2,512 ( V1 - V2 ) = V2
2,512 V1 - 2,512 V2 = V2
2,512 V1 = 3,512 V2
V2 = 0,715 V1
Soit Vb = V1 + V2 = 1,715 V1 = 0,1715 Va
Va + Vb = 500
1,1715 Va = 500
Va = 426,8 mL et Vb = 73,2 mL
Résolution exacte :
A l'aide de cette solution 0,2 mol.L-1 et d'une solution de soude à 2 mol.L-1, on veut préparer 500 mL de solution tampon de pH = 6. Quelles quantités des deux solutions faut-il mélanger ?
R1 = 10(pH-pK1) = 10(6-4,2) = 63,0957
R2 = 10(pH-pK2) = 10(6-5,6) = 2,5119
1 + R1 + R1R2 = 222,5851
[AH2] = C / ( 1 + R1 + R1R2) = 0,2*Va/500/222,5851= 1,7971 10-6 Va
[AH-] = C R1 / ( 1 + R1 + R1R2) = 63,0957 * 1,7971 10-6 Va = 1,1339 10-4 Va
[A2-] = C R1 R2 / ( 1 + R1 + R1R2) = 2,5119 * 1,1339 10-4 Va = 2,8482 10-4 * Va
[H3O+] = 10-pH = 10-6 mol.L-1
[OH-] =10-8 mol.L-1
C.M(Na) : [Na+] = 2 * Vb / 500 = 4 10-3 Vb
E.N : [Na+] + [H3O+] = [OH-] + [AH-] + 2 [A2-]
[AH-] + 2 [A2-] - [Na+] = [H3O+] - [OH-]
1,1339 10-4 Va + 2 * 2,8482 10-4 * Va - 4 10-3Vb = 9,9 10-7
6,8303 10-4 Va - 4 10-3 Vb = 9,9 10-7
Vb = 500 - Va
6,8303 10-4 Va - 4 10-3 (500-Va) = 9,9 10-7
6,8303 10-4 Va - 2 + 4 10-3 Va = 9,9 10-7
4,6830 10-3 Va - 2= 9,9 10-7
4,6830 10-3 Va = 9,9 10-7+ 2 = 2,00000099
Va = 2,00000099 / 4,6830 10-3
Va = 427,07 mL
Va = 427,1 mL
Vb = 72,9 mL
Le résultat obtenu par approximation est très proche du résultat exact.
Exercice 11 :
Soit un acide aminé symbolisé par
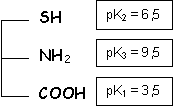
L'acidité la plus forte COOH réagit avec la base la plus forte NH2 et l'amphion de cet acide aminé est donc :
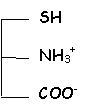
Soit le diagramme de prédominance :
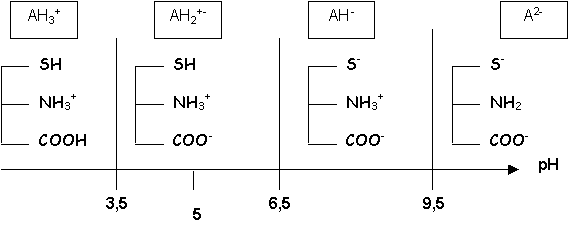
La concentration de l'amphion est maximale à pH = 1/2 ( pK1 + pK2 ) = 5 , c'est le pH d'une solution de cet acide aminé.
nAcAminé = 100 * 0,2 / 1000 = 0,02 mole
nsoude = 200 * 0,2 / 1000 = 0,03 mole
On voit qu'on à versé 1,5 fois plus de OH- que d'acide aminé (sous forme de l'amphion en solution). On a donc neutralisé totalement la première acidité de l'amphion et la moitié de la deuxième.

On a donc un pH proche du pK3 soit d'environ 9,5.
(Une résolution exacte conduit à pH = 9,500.)
Soit pour les concentrations :
C |
0,0667 |
pK1 |
3,5 |
pK2 |
6,5 |
pK3 |
9,5 |
pH |
9,5 |
R1 |
1000000 |
R2 |
1000 |
R3 |
1 |
AH3+ |
3,33E-11 |
AH2+- |
3,33E-05 |
AH- |
0,0333 |
A2- |
0,0333 |
nAcAminé = 100 * 0,2 / 1000 = 0,02 mole
nHCl = 200 * 0,1 / 1000 = 0,02 mole
On se trouve a la neutralisation exacte (point équivalent) de la basicité de l'amphion
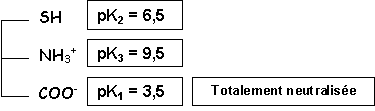
On a donc affaire à une solution d'un triacide faible.
Si on néglige les deux acidités les moins fortes on obtient
pH = 1/2 pK1 - 1/2 log C
C = 100 * 0,2 / 300 = 0,0667 mol.L-1
pH = 1/2 (3,5 - log 0,0667) = 2,34
(Une résolution exacte conduit à pH = 2,353)
Soit les concentrations :
C |
0,0667 |
pK1 |
3,5 |
pK2 |
6,5 |
pK3 |
9,5 |
pH |
2,3 |
R1 |
0,063095734 |
R2 |
6,30957E-05 |
R3 |
6,30957E-08 |
AH3+ |
0,0627 |
AH2+- |
0,00396 |
AH- |
2,496E-07 |
A2- |
1,575E-14 |